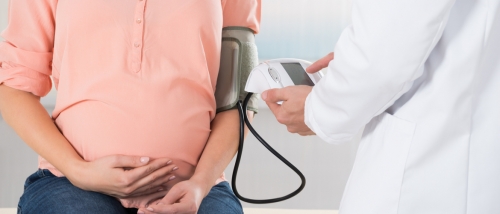
Aspectos atuais - tratamento cirúrgico da incôntinência urinária de esforço.
O tratamento da incontinência urinária de esforço (IUE) continua sendo um desafio, existindo inúmeras técnicas para a sua correção ao longo dos tempos.
Diferente de afecções que requerem técnicas que removem órgãos para sua resolução, o tratamento da IUE visa restabelecer uma função, reequilibrando os mecanismos de continência e evitando disfunções miccionais. Além disso, há de se considerar que muitos dos fatores de risco desencadeantes da IUE, como a obesidade, a tosse crônica e principalmente o envelhecimento, tecidual continuam atuando após a intervenção cirúrgica.
As técnicas mais utilizadas no tratamento da IUE são as colpofixações retropúbica (Burch ou Marshall–Marchetti–Krantz) e os slings, em especial os slings de uretra média1,2. Apesar da alta da taxa de sucesso da colpofixação retropúbica, o sling de uretra média é atualmente a técnica que apresenta as melhores e maiores evidencias científicas no tratamento desta afecção3,4,5.
A escolha da técnica a ser empregada não deve levar em conta apenas as taxas de sucesso, muito semelhantes segundo dados da literatura, mas também deve pesar os efeitos adversos de cada procedimento, considerando-se os riscos individuais de cada paciente, bem como a experiência do cirurgião4,6,7.
Os novos tratamentos cirúrgicos para a IUE, além de buscarem melhores resultados em longo prazo, apresentam características importante tais como: menor tempo de duração, menor agressão tecidual e recuperação mais rápida da paciente4.
Em 1996, Ulmsten et al.5 desenvolveram um novo procedimento para correção da incontinência urinária, o TVT (Tension-Free Vaginal Tape- Ethicon, Somerville, NJ, USA), que se trata de um sling de uretra média utilizando-se da via retropúbica para ancoragem, passível de realização ambulatorial. A base dessa cirurgia é a Teoria Integral da Continência, segundo a qual a correção do inadequado suporte uretral, por meio do reparo dos ligamentos pubouretrais e da parede vaginal suburetral, é essencial para a resolução dos sintomas de perda urinária.
Entre as características dessa cirurgia estão o fato da necessidade de mínima dissecção de parede vaginal, a aplicação de uma faixa específica de polipropileno, a ausência de tensão ao redor da uretra média, a não fixação da faixa e a possibilidade de ser realizada sob anestesia local, permitindo em grande parte das vezes que a paciente deixe o hospital no mesmo dia da cirurgia7,8,9.
Desde a criação desta cirurgia, desenvolveram-se inúmeros estudos, muitos deles multicêntricos, com o objetivo de avaliar suas taxas de cura e complicações. As taxas de cura variam de 74% a 95%, com seguimento de até 17 anos10,11,12,13,14. Cumpre ressaltar que esses trabalhos incluem pacientes com IU mista, com IUE recorrente e com deficiência intrínseca do esfíncter uretral12,13,14.
Em 2001, Delorme15 desenvolveu os slings de uretra média pela via transobturatória (TOT). A técnica é baseada na teoria de DeLancey16, que descreve a existência de uma fáscia pelviperineal e a oclusão da uretra sobre essa fáscia suburetral, pela pressão gerada pelo esforço.
Além disso, contrariamente à faixa colocada em posição retropúbica, a localização transobturadora da faixa, também de polipropileno, possibilita redução de risco de traumatismo visceral ou vásculo-nervoso. Não há risco de formação de hematoma no espaço de Retzius, e a incidência de disúria é menor, pela menor compressão uretral17. Os resultados mostram taxas de cura que variam entre 80% e 90%, no período de 12 meses17,18.
A técnica proposta por Delorme15, pela via transobturatória, compreende a inserção da faixa através do forâmen obturador de fora para dentro, ou seja, da raiz da coxa até a região suburetral (outside-in). Diante da ocorrência de lesões uretrais e vesicais com a aplicação dessa cirurgia, de Leval68 descreveu uma nova variação da técnica que permite a passagem da faixa através do forâmen obturador de dentro para fora (inside-out), com a utilização de instrumental específico. Essa técnica evitaria danos à uretra e à bexiga, tornando desnecessária a cistoscopia19.
De uma maneira global, as taxas de cura dos slings de uretra média pela via transobturatória variam de 81% a 100% com seguimento de 6 a 90 meses20,21,22.
Em metanálise com comparação entre as técnicas retropúbicas e transobturatórias foram demonstrados índices de cura equivalentes23.
Uma terceira geração de slings de uretra média tem sido desenvolvida nos últimos anos, com a finalidade de reduzir as complicações e adicionar simplicidade à técnica.
Seguindo a tendência mundial de adoção de procedimentos cada vez mais minimamente invasivos, surgiram os mini-slings ou slings de incisão única. Sua inovação consiste no uso de menor quantidade de material sintético e na ausência de orifícios cutâneos, com o intuito de reduzir o trajeto cego do procedimento para minimizar taxas de infecções e traumas viscerais24.
Diferentemente das técnicas já consagradas, os slings de incisão única disponíveis no mercado não são uniformes quanto a extensão da faixa, método de inserção bem como locais e formas de fixação. Acrescenta-se ainda a não uniformidade de técnicas cirúrgicas entre diferentes autores24. Portanto, os dados disponíveis a respeito de suas taxas de sucesso são conflitantes.
Em atualização de revisão sistemática seguida por metanálise, que avaliou 11 estudos comparativos entre os diferentes mini slings e slings retropúbicos ou transobturadores (1.702 pacientes), não foram observadas diferenças significantes entre as taxas de cura subjetiva ou entre as taxas de cura objetiva com tempo médio de seguimento de 18,6 meses24. Porém, é importante ressaltar que existe uma forte tendência dos slings retropúbicos terem uma taxa de sucesso maior que a via transobturatória24.
Assim, o sling retropúbico, o primeiro sling sintético de uretra média do qual se tem maior tempo de seguimento com altas taxas de cura e menos invasivo em relação às técnicas que o antecederam é uma boa opção para os casos mais graves de IUE, particularmente nas pacientes mais jovens. Por sua vez, o sling transobturador também está relacionado a altas taxas de cura, sendo o sling mais realizado em todo o mundo.
Já em relação aos slings de incisão única ou mini slings, faltam evidências quanto às taxas de cura e complicações em longo prazo para que tenham sua indicação definida. Porém, estão relacionados ao intraoperatório menos invasivo e ao pós-operatório imediato menos doloroso, podendo ser realizados apenas com anestesia local, sendo bem tolerados pela paciente.
Na ausência dos slings de uretra média, a cirurgia de Burch e os slings de aponeurose são opções com alta taxa de sucesso.
Autores:
Rodrigo de Aquino Castro1 e Raquel Martins Arruda2
- 1 - Professor Associado Livre Docente do Departamento de Ginecologia da Unifesp – EPM. Presidente da Comissão Nacional Especializada em Uroginecologia e Cirurgia Vaginal
- 2 -Chefe do Setor de Uroginecologia e Cirurgia Vaginal do Hospital do Servidor Público Estadual- São Paulo. Mestrado e doutorado pela Unisfesp-EPM
BIBLIOGRAFIA
- Serati M, Salvatore S, Uccella S, et al. Surgical treatment for female stress urinary incontinence: what is the gold-standard procedure? Int Urogynecol J Pelvic Floor Dysfunct. 2009;20(6):619-21.
- AUGS-SUFU Position Statement on Mesh Midurethral Slings for SUI. Disponível em: http://www.augs.org/d/do/2535 [accessed 25Jun14].
- Novara G, et al. Updated systematic review and meta-analysis of the comparative data on colposuspensions, pubovaginal slings, and midurethral tapes in the surgical treatment of female stress urinary incontinence. Eur Urol. 2010;58(2):218-38.
- Richter HE, et al. Retropubic versus transobturator midurethral slings for stress incontinence. N Engl J Med. 2010;362:2066-76.
- Ulmsten U, Henriksson L, Johnson P, et al. An ambulatory surgical procedure under local anesthesia for treatment of female urinary incontinence. Int Urogynecol J. 1996;7(2):81-6.
- Ulmsten U, Falconer C, Johnson P, et al. A multicenter study of Tension-Free Vaginal Tape (TVT) for surgical treatment of stress urinary incontinence. Int Urogynecol J. 1998;9(4):210-3.
- Nilsson CG, Palva K, Rezapour M, Falconer C. Eleven years prospective follow-up of the tension-free vaginal tape procedure for treatment of stress urinary incontinence. Int Urogynecol J. 2008;19(8):1043-7.
- Nilsson CG, Palva K, Aarnio R, et al. Seventeen year’s follow up of the tension free vaginal tape procedure for female stress urinary incontinence. Int Urogynecol J. 2013;24(8):1265-9.
- Rezapour M, Ulmsten U. Tension-free vaginal tape (TVT) in women with recurrent stress urinary incontinence- a long-term follow-up. Int Urogynecol J. 2001a;(Suppl 2):S 9-11.
- Rezapour M, Ulmsten U. Tension-Free vaginal tape (TVT) in women with mixed urinary incontinence--a long-term follow-up Int Urogynecol J Pelvic Floor Dysfunct. 2001;12(Suppl 2):S15-18.
- Rezapour M, Falconer C, Ulmsten U. Tension-Free vaginal tape (TVT) in stress incontinent women with intrinsic sphincter deficiency (ISD)--a long-term follow-up. Int Urogynecol J Pelvic Floor Dysfunct. 2001;12(Suppl 2):S12-14.
- Delorme E. La bandelette trans-obturatrice: um procédé mini-invasif pour traiter l’incontinence urinaire d’effort de la femme. Prog Urol. 2001;11:1306-13.
- DeLancey JOL. Structural support of the urethra as it relates to stress urinary incontinence: the hammock hypothesis. Am J Obstet Gynecol. 1994;170:1713-23.
- deTayrac R, Deffieux X, Droupy S, Chauveaud-Lambling A, Calvanèse-Benamour L, Fernandez H. A prospective randomized trial comparing tension-free vaginal tape and transobturator suburethral tape for surgical treatment of stress urinary incontinence. Am J Obstet Gynecol. 2004;190: 602-8.
- Roumeguère T, Quackels T, Bollens R, et al. Trans-obturator vaginal tape (TOT) for female stress incontinence: one year follow-up in 120 patients. Eur Urol. 2005;48:805-9.
- de Leval J. Novel surgical technique for the treatment of female stress urinary incontinence: transobturator vaginal tape inside-out. Eur Urol. 2003;44:724-30.
- Waltregny D, Gaspar Y, Reul O. TVT-O for the treatment of female stress urinary incontinence: results of a prospective study after a 3-year minimum follow-up. Eur Urol. 2008; 53:401-8.
- Abdel-Fattah M, Mostafa A, Familusi A et al. Prospective randomised controlled trial of transobturator tapes in management of urodynamic stress incontinence in women: 3 year outcomes from the evaluation of transobturator tapes study. Eur Urol. 2012;62:843-51.
- Athanasiou S, Grigoriadis T, Zacharakis D, Skampardonis N, Lourantou D, Antsaklis A. Seven years of objective and subjective outcomes of transobturator (TVT-O) vaginal tape: Why do tapes fail? Int Urogynecol J. 2014;25:219-25.
- Latthe PM, Singh P, Foon R, Toozs-Hobson P. Two routes of transobturator tape procedures in stress urinary incontinence: a meta-analysis with direct and indirect comparison of randomized trials.BJU Int. 2010;106:68-76.
- Deng DY, Rutman M, Raz S, Rodriguez LV. Presentation and management of major complications of midurethral slings: are complications under-reported? Neurourol Urodynam. 2007;26:46-52.
- Bianchi-Ferraro AM, Jarmy-Di Bella ZI, Castro Rde A et al. Single-incision sling compared with transobturator sling for treating stress urinary incontinence: a randomized controlled trial. Int Urogynecol J. 2013;24(9):1459-65.
- Djehdian LM, Araujo MP, Takano CC, Del-Roy CA, Sartori MG, Girão MJ, Castro RA. Transobturator sling compared with single-incision mini-sling for the treatment of stress urinary incontinence: a randomized controlled trial. Obstet Gynecol. 2014;123(3):553-61.
- Mostafa A, Lim CP, Hopper L, Madhuvrata P, Abdel-Fattah M. Single-incision mini-slings versus standard midurethral slings in surgical management of female stress urinary incontinence: an updated systematic review and meta-analysis of effectiveness and complications. Eur Urol. 2014;65(2):402-27.
Atendimento inicial à eclampsia.
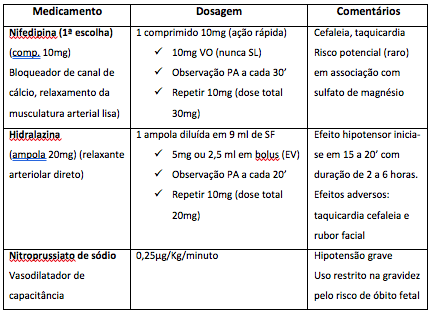
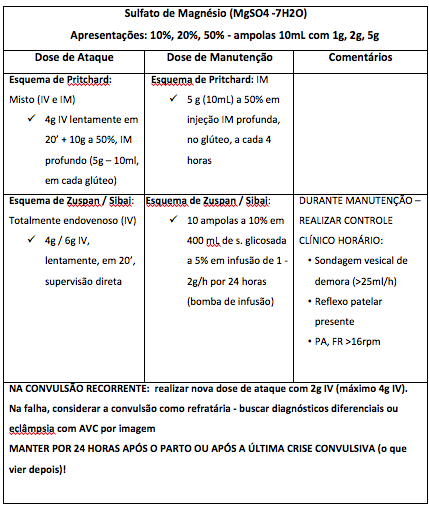 Quadro 3. Esquemas para administração de Sulfato de Magnésio para Eclâmpsia
Quadro 3. Esquemas para administração de Sulfato de Magnésio para Eclâmpsia - Deve ser realizada, para uma unidade de maior complexidade ou para a UTI apenas após estabilização da paciente;
- Aceitação do caso pela unidade que irá receber, após comunicação adequada de todos os detalhes do caso;
- Veículo adequado para o transporte;
- Acesso venoso e hidratação controlada;
- Terapia anticonvulsivante instalada (de acordo com a distância e disponibilidade de infraestrutura para transferência – se grandes distâncias e sem condições de uso de bombas de infusão=> sulfato de magnésio dose de ataque pelo Esquema de Pritchard IV + IM, para reduzir risco de infusão intempestiva durante o transporte - OMS, 2011);
- Anti-hipertensivos de emergência preparados;
- Acompanhamento por médico;
- Material para intubação, ventilação e reanimação
Gestação de alto risco baseada em evidências. Santos el al, 2011 MED BOOK EDITORA CIENTIFICA LTDA
Herpes simples.
Brunella Cesconetto Grillo
Graduada pela Universidade Brasileira de Vitória, UNIVIX, Residência médica pelo Hospital Universitário Cassiano Antonio Moraes (HUCAM) da UFES, pós graduação em medicina infanto puberal pela UNIRIO e preceptora do ambulatório de infanto puberal do centro de especialidades Unimed Vitória, ES
Neide Aparecida Tosato Boldrini
Professora adjunta de Ginecologia e obstetrícia da UFES, médica do ambulatório de Patologias do Trato genital inferior e colposcopia do HUCAM-UFES, Doutorado em doenças infecciosas pela UFES e presidente da ABPTGIC-ES.
A infecção pelo Vírus Herpes Simples (HSV) é a principal causa de úlcera genital em todo o mundo, sendo o HSV-2 o sorotipo mais frequentemente implicado na sua etiologia. É doença infectocontagiosa, crônica e generalizada, sujeita a recidivas, tendo como agente etiológico duas cepas diferentes do vírus herpes simples, o tipo 1 (HSV-1) e o tipo 2 (HSV-2). Seu período de incubação varia de 1 a 26 dias após o contágio, sendo a média de 7 dias. A infecção e a reativação podem ser assintomáticas, e a transmissão ocorre predominantemente pelo contato sexual, podendo também ser transmitido da mãe para o filho durante o parto. O contato com lesões ulceradas ou vesiculadas é a via mais comum.
Herpes e HIV
O herpes genital está associado a um risco duas a três vezes maior de aquisição do HIV, podendo ser responsável por 40 a 60% das novas infecções pelo HIV em uma população com alta prevalência pelo HSV. O sinergismo entre a infecção pelo HSV-2 e a infecção pelo vírus da imunodeficiência adquirida (HIV) resulta em um aumento da frequência das reativações do HSV-2 em indivíduos HIV-positivos. Por outro lado, a infecção pelo HSV-2 aumenta o risco de aquisição do HIV e acelera a própria progressão da doença. Além disso, os indivíduos soropositivos para HSV-2 são mais propensos à forma sintomática da doença, incluindo surtos mucocutâneos mais freqüentes e mais graves.
Nos indivíduos coinfectados pelo HIV, os aspectos clínicos são assiduamente atípicos, podendo-se observar úlceras extensas, atípicas, graves e as quais tendem para a cronicidade com sobreinfecção bacteriana. Mais raramente, tem sido descritas formas hipertróficas pseudotumorais as quais simulam carcinoma espinocelular ou outras infecções virais (Figura 1).
A coinfecção HSV/HIV ocorre em 50 a 95% dos indivíduos, segundo estudos realizados em diferentes partes do mundo. Os vírus herpes simples constituem uma grande causa de morbidade em indivíduos imunodeprimidos.
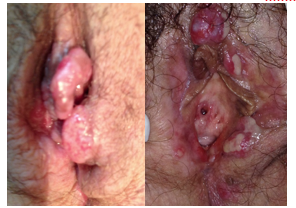
Figura 1. Lesão herpética hipertrófica em paciente HIV positiva. À esquerda observa-se aspecto tumoral inicial, após 10 dias da biópsia a lesão persistiu com aspecto ulcerado (à direita), no exame histopatológico frequentes células escamosas exibindo efeito citopático pelo vírus herpes.
Epidemiologia
O herpes genital é infecção comum e ascendente, tanto em países industrializados como naqueles em desenvolvimento. A grande maioria dos casos é causada pelo HSV-2, embora a prevalência do HSV-1 encontre-se em ascensão, principalmente na população jovem, devido à prática de sexo oral.
A infecção por HSV-2 é um problema mundial, e se calcula que haja no mundo 400 milhões de pessoas infectadas. Em 2012, a prevalência estimada da infecção era mais elevada na África (31,5%), seguida das Américas (14,4%). Há mais mulheres que homens infectados por HSV-2: 267 e 150 milhões, respectivamente, segundo estimativas de 2012. Nos grupos etários em que há início precoce de atividade sexual, as taxas de prevalência para HSV-2 chegam a 30% em adultos.
O HSV, A LATÊNCIA E REATIVAÇÃO.
Os HSV apresentam fenômeno biológico único, a capacidade de latência e de posterior reativação. Após uma primoinfecção, o vírus permanece em determinadas células sem provocar qualquer sintomatologia no hospedeiro, podendo ser reativado e, de novo, produzir viriões. Esta reativação pode ser sintomática ou não e é uma nova oportunidade de disseminação do HSV; a infecção torna-se crônica e tende a aumentar a prevalência. Os locais de latência variam: os vírus dermoneurotrópicos (HSV e VZV), após a primoinfecção, deslocam-se através da bainha periaxonial dos nervos sensitivos até atingirem os gânglios nervosos sensitivos correspondentes à região atingida. As células com HSV latente não se dividem, por isso não há produção de proteínas virais, o genoma do vírus comporta-se como se estivesse “desligado”.
Pacientes com deficiência de IgA apresentam ulcerações recorrentes da mucosa oral e, com frequência, infecções herpéticas. Fatores externos, como a exposição solar, a exposição a ambientes quentes ou frios; fatores internos, como a fadiga, o stress psicológico, o período menstrual, a relação sexual, a imunodepressão, a administração de corticosteróide, a febre, a cirurgia por laser, traumas teciduais localizados ou alteração na atividade antiviral da saliva desencadeiam a reativação. Também são mencionadas reações alérgicas, administração de adrenalina ou de hormônios hipofisários e emoções.
SINTOMATOLOGIA.
Quando sintomática, a primoinfecção é precedida por um pródromo, focalizado na zona da futura lesão, com dor, ardência e sensação de “formigamento”; estes sintomas duram cerca de 24 horas. A primoinfecção estabelecida manifesta-se inicialmente por cefaléia, febre, mal-estar e adenopatia inguinal, sintomas que costumam desaparecer antes da cura das lesões. Estas surgem 4 a 7 dias depois do início da infecção, sob a forma de vesículas dolorosas, de dimensão variável: na mulher, nos pequenos lábios, na vulva, na vagina e no trato urinário, podendo também atingir o colo do útero; no homem, no pênis, podendo também atingir o escroto. Na primoinfecção as lesões podem ser muito dolorosas e ocorrer também disúria e dificuldade de andar, mais comuns em mulheres, afetando psicologicamente a paciente. As vesículas rompem depois, ulceram e formam-se crostas sobre as lesões que curam, em geral sem deixar cicatrizes, em 2 a 6 semanas.
A persistência de lesões por várias semanas, ou o surgimento de novas lesões, pode levar o clínico a suspeitar de imunodepressão e a requerer os ensaios respectivos. Retenção urinária ocorre em 10-15% das pacientes do sexo feminino.
A gravidade da infecção primária parece estar relacionada com a frequência de recorrências, isto é, quanto mais grave a infecção primária, mais prováveis e frequentes serão as recorrências. Os portadores de HIV podem apresentar episódios de infecção mais prolongados e mais graves.
A complicação local mais comum é a infecção bacteriana secundária, mas podem surgir complicações sistêmicas, como a meningite asséptica, radiculomielite sacral e neuralgia. Esta é rara em homens, mas, em mulheres pode atingir 25% a 30% dos casos de primoinfecção.
DIAGNÓSTICO
1.Diagnóstico Clínico
O diagnóstico do herpes genital é essencialmente clínico, baseado na história médica e exame físico. Entretanto, em alguns casos, o diagnóstico clínico pode ser pouco sensível e inespecífico. As lesões típicas causadas pelo HSV (múltiplas, dolorosas, vesiculares ou ulcerativas) podem estar ausentes em muitas das pessoas infectadas.
A infecção primária e recorrente pelo HSV se faz habitualmente acompanhar de linfoadenopatia inguinal dolorosa e móvel.
2.Detecção direta do HSV.
Deve-se coletar o material das lesões com um swab de algodão ou dacron. Uma alternativa é a aspiração das vesículas intactas com agulha fina, pois os vírions são abundantes neste fluido. As amostras devem ser colocadas imediatamente em um meio de conservação/transporte adequado.
3.Citopatologia (Método de Tzanck).
Trata-se de um raspado do assoalho de uma vesícula íntegra com uma lâmina e cora-se pelo método de Giemsa, Wright ou Hematoxilina-eosina ou pelo Papanicolau; permite a observação de inclusões virais, que podem ser observadas em 50% dos casos. A positividade é dada pela presença de multinucleação e balonização celulares.
4.Testes virológicos.
O isolamento do HSV em cultura de células em pacientes que apresentam lesões genitais ulceradas ou outras lesões mucocutâneas
5.Testes para detecção de antígenos para o HSV.
Utilizado especialmente em pacientes que apresentam imunodeficiência. Pode ser detectada tanto por imunofluorescência com fluoresceína conjugada a anticorpo anti-HSV, como por ensaio imunoadsorvente ligado à enzima (ELISA). É possível realizar-se a tipagem viral através de anticorpo monoclonal.
Os testes de Polymerase Chain Reaction (PCR) do DNA do HSV são altamente sensíveis. A técnica de PCR está disponível e constitui o teste de eleição para o diagnóstico de infecção pelo HSV no sistema nervoso central (pesquisa de HSV em líquido cefalorraquiano) onde a titulação viral é baixa.
6.Hibridização do DNA-HSV.
A hibridização do DNA-HSV é utilizada, em particular, nos pacientes imunocomprometidos.
7.Testes sorológicos tipo-específicos para o HSV.
Anticorpos tipo-específicos e não específicos para o HSV se desenvolvem durante as primeiras semanas que se seguem à infecção pelo HSV e persistem indefinidamente. Estes testes se baseiam na presença de anticorpos contra as glicoproteínas G1 e G2 do HSV, que têm especificidades antigênicas para o HSV-1 e HSV-2, respectivamente.
O Western Immunoblot (WBA), que detecta anticorpos contra proteínas virais, e o Ensaio Imunoenzimático (EIA), que detecta anticorpos tipo-específicos contra a glicoproteína G, são testes sorológicos tipo-específicos, extremamente sensíveis e específicos. Entretanto, não há indicação de triagem para o HSV-1 e HSV-2 na população geral.
TRATAMENTO
A abordagem geral do tratamento, para cada caso, inclui a prevenção da transmissão, a atenuação da sintomatologia, a redução da possibilidade de complicações posteriores, a promoção da cura do episódio e a supressão possível dos episódios de recrudescência. Se os sintomas forem mínimos, poderá ser suficiente a utilização de analgésicos e de limpeza das lesões.
Para o primeiro episódio clínico, que tende a ser mais prolongado, com úlceras mais severas, podendo até conter acometimento neurológico, é recomendado tais esquemas; Aciclovir 400mg 3 vezes ao dia por 7-10 dias; Aciclovir 200 mg 5 vezes ao dia por 7-10 dias ou Valaciclovir 500 mg 2 vezes ao dia por 7-10 dias ou ainda Fanciclovir 250 mg 3 vezes ao dia por 7-10 dias.
A terapia supressiva tem como função reduzir a frequência das recidivas e melhorar ou amenizar a gravidade das lesões. Esta diminui a recorrência do herpes genital em 70-80%. A segurança e a eficácia foram documentadas entre pacientes que usam dose diária de Aciclovir por até 6 anos e Valaciclovir e Fanciclovir por 1 ano. Tais esquemas podem ser utilizados: Aciclovir 400 mg/dia; Valaciclovir 500mg- 1g/dia; Fanciclovir 250 mg/dia.
O uso diário de 500mg de Valaciclovir diminui a taxa de transmissão do HSV-2 em casais heterossexuais, funcionando também como uma estratégia para prevenir transmissão, além do uso do preservativo e evitar a atividade sexual durante as recorrências. A terapia supressiva também reduz a transmissão de pessoas com múltiplos parceiros, incluindo pessoas soropositivas para HSV-2 sem herpes genital. O tratamento do herpes genital recorrente, para ser efetivo, necessita ser iniciado no primeiro dia da lesão ou nos pródromos.
A transmissão neonatal é elevada (30-50%) para as gestantes que adquirem herpes próximo ao parto e menor de 1% para as que adquirem no primeiro trimestre. Mulheres sem o diagnóstico de herpes genital devem evitar ter relações sexuais, principalmente no terceiro trimestre, com parceiros sabidamente infectados. Testes sorológicos podem ser úteis na identificação dessas gestantes com risco de infecção. Embora o parto cesariano não elimine completamente o risco de transmissão neonatal, este deve ser recomendado caso a gestante apresente lesão herpética no início do trabalho de parto.
O Aciclovir pode ser usado para o tratamento do herpes genital em qualquer fase da gravidez, até naquelas que estão amamentando. Embora os dados sobre o uso gestacional do Valaciclovir e do Fanciclovir sejam limitados, estudos em animais demonstraram baixo risco em mulheres grávidas. O tratamento supressivo com Aciclovir reduz a taxa de cesareana, por diminuir a recorrência das lesões; porém, não reduz a transmissão neonatal.
O regime supressivo recomendado sugere que o tratamento seja iniciado a partir de 36 semanas de gestação com Aciclovir 400 mg 3x ao dia ou Valaciclovir 500mg/dia.
O tratamento intravenoso é reservado para as doenças severas ou suas complicações (pneumonite, encefalite e doenças disseminadas). A terapia anti-retroviral reduz a gravidade e a freqüência dos sintomas do herpes genital. As manifestações clínicas do herpes genital podem piorar durante a reconstituição imune logo após o início da terapia anti-retroviral.
Frequentemente, o herpes genital hipertrófico é refratário aos antivirais sistêmicos de primeira linha, tais como o Aciclovir (oral e endovenoso), o Valaciclovir e o Fanciclovir. Todas as estirpes resistentes ao Aciclovir, são também resistentes ao Valaciclovir e ao Fanciclovir. Nestes casos, o Foscarnet 40-80 mg/kg intravenoso, até a resolução clínica, deve ser aventado; assim como o Interferon-beta e Cidofovir 5 mg/kg uma vez por semana.
Ainda que não existam estudos randomizados, parece eficaz o uso do Imiquimod (imunomodulador tópico, com atividade antitumoral e antiviral que induz a síntese e libertação de várias citocinas endógenas pró-inflamatórias TH-1, nomeadamente de Interferon-alfa).
O Imiquimod deve ser aplicado nas lesões uma vez ao dia por 5 dias consecutivos. Outras drogas encontram-se ainda sob avaliação da sua eficácia, como a Trifluorotimidina, a Vidarabina e o Cidofovir, podendo ser utilizadas em casos especiais.
Autora:
Brunella Cesconetto Grillo
REFERÊNCIAS BIBLIOGRÁFICAS.
1 - Gubinelli E, Cocuroccia B, Lazzarotto T, Girolomoni G. Nodular perianal herpes simplex with prominent plasma cell infiltration. Sex TransmDis. 2003;30:157-9.
2 - Wald A, Link K. Risk of human immunodeficiency virus infection in herpes simplex virus type 2-seropositive persons: a meta-analysis. J InfectDis 2002; 185:45-52.
3 - Looker K, Garnett G. An estimate of the global prevalence and incidence of herpes simplex virus type 2 infection.Public health reviews. Bulletin of the World Health Organization 2008; 86:805-12.
4 - McCormack S, Walsh JC, Barton SE, Kiffer CRV. Herpes Simples. In: Focaccia R, editor. 3a ed. Tratado de Infectologia. São Paulo: Atheneu, p. 549-67, 2005.
5 - Samaratunga H, Weedon D, Musgrave N, McCallum N. Atypical presentation ofherpes simplex (chronic hypertrophic herpes) in a patient with HIV infection.Pathology. 2001;33:532-5.
6 - Foley E, Patel R. Treatment of genital herpes infections in HIV-infected patients. J HIV Ther 2004; 9:14-8.
7 - Looker K, Garnett G. An estimate of the global prevalence and incidence of herpes simplex virus type 2 infection. Public health reviews. Bulletin of the World Health Organization 2008; 86:805-12.
8 - Glasier A, Gulmezoglu AM, Schmid GP, Moreno CG, Van Look PF. Sexual and reproductive health: a matter of life and death. Lancet 2006; 368:1595-607.
9 - CDCP. (2014). Sexually Transmitted Diseases; Treatment Guidelines, 2010.Centers for Disease Control and Prevention. Atlanta, EUA. [Emlinha].Disponivelemhttp://www.cdc.gov/std/treatment/2014/genitalulcers.htm
10 - Strauss, E. e Strauss, J.(2002). Viruses and Human Disease. Academic Press, California.
11 - Howley, P. e Knipe, D. (2007). Fields Virology, Vol I. 5 th Edition. LippincottWilliam&Wilkins, Philadelphia.
12 - Sen P, Barton SE. Genital herpes and its management. BMJ 2007; 334:1048-52.
13 - Rana RK, Pimenta JM, Rosenberg DM et al. Sexual behaviour and condom use among individuals with a history of symptomatic genital herpes. Sex Transm Infect 2006; 82:69.
14 - Workowski KA, Berman MS. Sexually Transmitted Diseases Treatment Guidelines, 2006. MMWR Recomm Rep 2006 (RR-11); 55:1-95.
15 - Corey L, Bodsworth, N, Mindel A et al. An update on short-course episodic and prevention therapies for herpes genitalis. Herpes 2007; 14 (Suppl. 1):5A.
16 - Kudesia, G. e Wreighitt,T. (2009). Clinical and Dignostic Virology.CambridgeUniversity Press, Cambridge.
17 - Duque V, Malcata L, Serra E et al. Doenças infecciosas: o desafio daclínica. 2008; 53-56,130-131.
18 - Fatahzadeh M. e Schwartz, R. (2007). Human Herpes Simplex Virus Infections:Epidemiology, Pathogenesis, Symptomatology, Diagnosis and Management. AmericanAcademy of Dermatology, Inc.,57, pp. 737-761.
19 - Veronesi R, Focaccia R. Tratado de Infectologia. 1997; 25:85-399.
BIOMARCADORES MOLECULARES NA PROGRESSÃO DA LESÃO PRECURSORA PARA O CÂNCER DO COLO UTERINO
INTRODUÇÃO:Na maioria dos países em desenvolvimento, o câncer do colo uterino lidera as causas de morte por neoplasia entre as mulheres¹. No Brasil, este tumor é o terceiro mais frequente na população feminina, atrás do câncer de mama e do colorretal, e a quarta causa de morte de mulheres por câncer no Brasil. Sendo assim, o controle na incidência desta doença é uma questão de saúde pública e os estudos que contribuem para o conhecimento da carcinogênese do colo uterino irão nos ajudar neste controle².
Já está estabelecido que sobre certas circunstâncias, a infecção persistente com um tipo oncogênico de Papilomavírus humano (HPV) é a condição necessária para o desenvolvimento das lesões precursoras e do câncer cervical.
O HPV é considerado pela Organização Mundial de Saúde (OMS) o agente etiológico do câncer do colo uterino, evidenciado por meio de estudos epidemiológicos e moleculares.¹ Entretanto, a infecção causada pelo HPV isoladamente não é suficiente para o aparecimento das lesões precursora e invasora do colo uterino. Fatores endógenos relacionados ao hospedeiro (p.ex. hormônios endógenos, fatores genéticos e resposta imune) e exógenos ambientais (p.ex. anticoncepcional oral, tabagismo, dieta e multiparidade) e virais (p.ex. tipos oncogênicos e variantes do HPV) aumentam o risco de aparecimento desta lesão.³-4
BIOMARCADORES TUMORAIS
Nos últimos anos, o estudo dos mecanismos genéticos e moleculares, implicados na gênese e na progressão do câncer, tem permitido obter novos métodos diagnósticos e de acompanhamento. O câncer apresenta como característica a proliferação celular não controlada e anormalidades em genes, que regulam o ciclo celular, podem ser encontrados em vários tipos de tumor.5-6
Estudos recentes em biologia molecular mostraram que o desenvolvimento de tumores envolve, basicamente, duas classes de genes: os proto-oncogenes e os genes supressores de tumor. Os proto-oncogenes (p.ex. rás e c-myc) estão associados à regulação da proliferação celular. Os genes supressores tumorais (p.ex. Rb, TP53 e p16INK4a) estão associados ao controle negativo do ciclo de divisão celular.7 Evidências sugerem que estes genes quando alterados, ou expressos impropriamente, podem induzir ao processo oncogênico. A inativação de genes supressores de tumor está entre os mecanismos genéticos mais comuns envolvidos na transformação maligna.8
Além das alterações genéticas encontradas no processo de oncogênese, alterações epigenéticas são também descritas no DNA humano. Estas, diferentemente das alterações genéticas, não alteram definitivamente o código genético, ou seja, ocorre mudança no padrão de expressão do gene sem haver alteração na seqüência de bases nitrogenadas do DNA.
Tais eventos são considerados por muitos pesquisadores como ponto chave no desenvolvimento do câncer, porque estas alterações ocorrem em todos os estágios de formação dos tumores, incluindo as fases precoces e têm sido reconhecidas como o principal mecanismo envolvido na inativação dos genes supressores de tumor. As duas principais alterações epigenéticas descritas são a metilação do DNA e a deacetilação das histonas. Estas duas alterações epigenéticas são de controle transcricional e estão integralmente ligadas.9
A metilação é a modificação química do gene, de controle da integridade e expressão gênica, mediada por enzimas, onde um grupamento metil (CH3) adicionado à citosina localizada nos carbonos 5 de bases guanimas (G), conhecidas como ilhas CpG, forma a metilcitosina.10 A enzima que catalisa esta modificação química é da família das DNA metiltransferases (DNMT).9
A metilação está estabelecida como um dos marcadores moleculares mais importantes dos tumores humanos. Esta alteração é responsável por causar mudanças em genes que têm importância no desenvolvimento do câncer, como por exemplo, nos genes de reparo do DNA, da apoptose e dos que interferem com a progressão do ciclo celular.12
O principal achado de inativação na transcrição genética por hipermetilação é o do gene p16INK4a. Este gene é mapeado na banda p21 do cromossomo 9. Sua função é de suprimir o crescimento tumoral através do controle negativo do ciclo de divisão celular.5 A proteína p16 inibe as CDK4 e 6 no ponto de checagem G1, para que a célula entre na fase G0 (quiescência) até que um dano ocorrido no DNA seja corrigido. A inativação desta proteína ou a sua ausência (por metilação do gene p16INK4a) permite que a célula entre na fase S após uma breve parada na fase G1, sem restauração das alterações do DNA.5
A proteína p16 tem recebido atenção especial como um biomarcador de diagnóstico de lesões intraepiteliais escamosas cervicais, com o potencial de ser usada como ferramenta de rastreamento adicional.12
A superexpressão da proteína p16 nas neoplasias cervicais tem sido associada com a infecção por HPV. De fato, a proteína E7 do HPV oncogênico é responsável pelo aumento dos níveis de expressão de proteína p16. De acordo com esta hipótese, a disfunção da proteína pRb através da associação com a proteína E7 do HPV, aumenta a liberação do fator de transcrição E2F resultando em superexpressão da proteína p16 e progressão anormal do ciclo celular.12
Metilação aberrante do gene 16ÍNK4a ocorre, precocemente, na população de células tumorais em lesões cervicais escamosas precursoras ou invasoras, numa freqüência que varia de 10 a 100%. A perda da transcrição do gene p16INK4a anula o mecanismo de controle negativo da proteína p16, que desvia células com DNA danificado do ciclo celular, podendo favorecer o descontrole na proliferação celular. Esta pode ser considerada uma das bases da oncogênese humana. Na carcinogênese do colo uterino, além da mutação do DNA induzida pela integração do HPV, tem sido observado frequente hipermetilação do gene p16INK4a.9
Nuovo et al (1999)13, utilizando PCR metilação especifica de hibridização in situ (MSP-ISH), detectaram em espécimes arquivados metilação do gene p16 em células isoladas de carcinoma escamoso do colo uterino. Estudaram, também, por imunohistoquímica a expressão da proteína p16 em relação ao estado de metilação. Demonstraram hipermetilação da região promotora do gene p16ÍNK4a nos casos de carcinoma escamoso e nas áreas periféricas com lesão escamosa intra-epitelial de alto grau e ausência da proteína nestes casos. Os autores sugerem que a inativação do gene p16, por metilação excessiva, pode cancelar a aparente proteção da hiperexpressão de proteína p16, que bloquearia a proliferação desordenada de células com instabilidade do genoma pela integração do DNA-HPV nas lesões cervicais.
Virmani et al (2001)14 descreveram presença de metilação do gene p16 nas lesões precursoras e invasoras cervicais. Os autores demonstraram que a metilação estava completamente ausente no grupo controle e era evento raro no grupo com lesão de baixo grau. Sugeriram que a presença de metilação aberrante no gene p16 pode auxiliar a identificar um subgrupo com risco aumentado para progressão histológica da lesão.
A importância das alterações epigenéticas reside no fato de que elas podem ser revertidas pelo emprego de pequenas moléculas, se constituindo em alvos promissores para o desenvolvimento de drogas ou mudanças dietéticas para a prevenção e o tratamento de câncer. Já existem drogas que atuam na metilação. As mais conhecidas são a 5-azacytidine (5-aza-CR) e 5-aza-doxycydine (5-aza-CdR). São drogas que poderão melhorar o prognóstico do paciente de câncer, principalmente se forem instituídas em fases precursoras ou precoces do câncer do colo uterino.15-16
Outras drogas que mostraram ser capazes de reativar a transcrição do gene p16INK4a foram a procainamida (usada para tratamento de arritmias cardíacas), procaína (anestésico) e a hidralazina (droga anti-hipertensiva). As duas primeiras agem através de inibição da atividade da DNMT (testada em células de câncer de próstata, em experiências usando ratos) e a terceira tem sua ação na diminuição da transcrição do RNAm das DNMT (mostrou demetilar o gene ERβ in vitro em linhagens de células de câncer de mama, melhorando a resposta ao tamoxifeno).16
CONCLUSÃO:
A inativação do gene p16INK4a desenvolve um processo hiperproliferativo por descontrole do ciclo celular e parece predispor a célula a responder com mutações a eventos moleculares oncogênicos.5
Estudos genéticos e epigenéticos poderão nos fazer identificar as neoplasias do colo uterino com maior chance de progressão ou de recidiva, porque apenas a imortalização dessas células epiteliais pelos oncogenes virais não é suficiente para explicar a carcinogênese.5
Autores:
Yara Lucia Mendes Furtado De Melo
Professora adjunta da UFRJ e UNIRIO, coordenadora da graduação da UFRJ, presidente da Associação Brasileira de Patologia do Trato Genital Inferior e Colspocopia - capítulo RJ.
Referencias:
- Bosch FX e Sanjosé S. Chapter 1- Human papillomavirus and cervical cancer: burden and assessment of causality. J Natl Cancer Inst Monogr, 2003;3:3- 13.
- INCA - Instituto Nacional do Cancer – Tipos de Cancer: Rio de Janeiro, INCA, 2017. Disponível em: http://www2.inca.gov.br/wps/wcm/connect/tiposdecancer/site/home/colo_utero >. Acesso em: 06.09.2017.
- Acladious NN; et al. Persistent human papillomavirus infection and smoking increase risk of treatment of cervical intraepithelial neoplasia (CIN). Int J Cancer.2002; 98:435-9.
- Castellsagué X e Muñoz N. Chapter 3- Cofactors in Human papillomavirus carcinogenesis-Role of parity, oral contraceptives, and tobacco smoking. J Natl Cancer Inst. Monogr.2003;31:20- 8.
- Furtado YL, Almeida G, Lattario F, Silva KS, Maldonado P, Silveira FA, do Val IC, Fonseca R, and Carvalho MGC. The Presence of Methylation of the p16INK4A Gene and Human Papillomavirus in High-grade Cervical Squamous Intraepithelial Lesions. Diagn Mol Pathol 2010;19(1):15-9
- Yang HJ; et al. Detection of hypermethylation genes in tumor and plasma of cervical cancer patients. Gynecol Oncol.2004;93:435- 40.
- Sugerman PB; Joseph, BK; Savage, NW. The role of oncogenes, tumour suppressor genes and growth factors in oral squamous cell carcinoma: a case of apoptosis versus proliferation. Oral Dis.2005;1:172-88.
- Reed AL; et al. High frequency of p16 (CDKN2/MTS-1/INK4A) inactivation in head and neck squamous cell carcinoma. Cancer Res.1996;56:3630-3.
- Duenas-gonzalez A; et al. Epigenetics of cervical cancer. An overview and therapeutic perspectives. Mol Cancer.2005;4:38-61.
- Herman JG; et al. Methylation-specific PCR: a novel PCR assay for methylation status of CpG islands. Proc Natl Acad Sci U S A.1996;93(18):9821-6.
- Baylin SB e Herman, JG. DNA hypermethylation in tumorigenesis. Trends Genet.2000;16(4):168-74.
- Murphy N; et al. P16INK4a, CDC6, and MCM5: predictive biomarkers in cervical preinvasive neoplasia and cervical cancer. J Clin Pathol.2005;58:525-34.
- Nuovo GJ; et al. In situ detection of the hypermetylation-induced inactivation of p16 gene as an early event in oncogenesis. Proc Natl Acad Sci USA.1999;96(22): 12754-9.
- Virmani AK; et al. Aberrant methylation during cervical carcinogenesis. Clin Cancer Res.2001;7(3):584-9.
- Jones PA e Baylin, SB. The fundamental role of epigenetic events in cancer. Nature.2002;3:415-28.
- Lu Q; et al. Epigenetics, disease, and therapeutic interventions. Ageing Res Rev, v. 5, p. 449-467, 2006.
Terminologia LAST
Com o objetivo primordial de revisar e uniformizar a terminologia diagnóstica das lesões epiteliais escamosas HPV-induzidas do trato anogenital inferior, o Projeto LAST (“Lower Anogenital Squamous Terminology”) contou com a participação de especialistas do Colégio Americano de Patologia (CAP) e da Sociedade Americana de Colposcopia e Patologia Cervical (ASCCP), e publicou suas recomendações no final de 2012 em periódicos direcionados a diferentes públicos-alvo, incluindo ginecologistas e patologistas.
A recomendação principal do Consenso LAST é a de que, independentemente da topografia em questão (colo uterino, vagina, vulva, períneo, pênis, região escrotal, perianal ou canal anal), a terminologia diagnóstica utilizada seja de duas categorias que refletem as categorias biológicas das lesões morfológicas HPV-induzidas, a saber:
(1) lesão intraepitelial escamosa de baixo grau - LIEBG - infecção produtiva de partículas virais, de menor risco biológico - na qual geralmente pode se observar células proliferantes sem atipias significativas acometendo o terço basal do epitélio, associadas à maturação com numerosas células exibindo atipias coilocitóticas nas camadas mais superficiais, sem atividade mitótica na metade superficial do epitélio
(2) lesão intraepitelial escamosa de alto grau LIEAG - lesão proliferativa de células epiteliais relacionada a infecção transformante neoplásica, de maior risco biológico - caracterizada geralmente por marcante proliferação de células com maior desorganização, perda de polaridade, atipias e atividade mitótica significativas, já acometendo o terço médio ou a metade superficial do epitélio e podendo ocupar toda a sua espessura, associadas a perda de maturação epitelial e a atipias coilocitóticas menos extensas ou mesmo não detectáveis.
A fim de realizar uma correlação com a terminologia diagnóstica de neoplasia intraepitelial (NI-) universalmente utilizada, inclui-se entre parênteses o termo NI-1 nos casos de LIEBG e os termos NI-2/3 ou NI-3 nos casos de LIEAG.
Em lesões classificadas como NI-2 (particularmente NIC 2, com dificuldade de distinção entre LIEBG e LIEAG, considerada como categoria de significado biológico mais incerto), estaria indicada propedêutica complementar na tentativa de se melhor avaliar o seu risco biológico - de maneira similar à realização de testes de HPV em interpretações citológicas de ASC-US.
A utilização de outras terminologias mais antigas e epônimos deve ser evitada, assim como o termo carcinoma espinocelular microinvasivo (substituído por carcinoma espinocelular superficialmente invasivo - que corresponderia a Estádio FIGO IA1 no caso do colo uterino).
Outra importante recomendação do Consenso LAST é a inclusão de estudo imuno-histoquímico como método complementar ao exame anátomo-patológico no fluxograma diagnóstico.
Nas infecções transformantes por HPV de alto risco oncogênico, a inativação funcional da pRb pela oncoproteína viral E7 desencadeia superexpressão da proteína p16, a qual pode ser detectada por método imuno-histoquímico.
A utilização de estudo imuno-histoquímico complementar com p16 (assim como a aplicação de terminologia diagnóstica de 2 categorias) aumenta os índices de concordância inter- e intra-observador na avaliação de espécimes histopatológicos de colo uterino. É o único marcador oficialmente validado pelo Consenso “LAST”, sendo a sua utilização indicada nas seguintes situações:
(1) amostras em que há dúvida no diagnóstico diferencial entre lesão pré-cancerosa versus condição benigna (isto é, epitélios escamosos imaturos, geralmente cervicais e metaplásicos, com atipias);
(2) casos em que o patologista está considerando a interpretação diagnóstica de NIC 2 (na qual a positividade para o marcador favoreceria tratar-se de lesão potencialmente não-regressiva, com maior probabilidade de LIEAG, e a negatividade para o marcador favoreceria tratar-se de lesão de menor risco biológico, possivelmente LIEBG de morfologia mais atípica);
(3) situações em que há discordância diagnóstica entre dois profissionais analisando o espécime, e cujo diagnóstico diferencial inclui lesão pré-cancerosa.
Seu uso em amostras com NI-3 é contra-indicado, sendo também não recomendado para amostras não neoplásicas ou com NIC 1 (nestas duas últimas morfologias, exceto em situação de risco elevado para sub-diagnóstico de lesão importante, a saber: exame citológico prévio com interpretação de LIEAG, ASC-H, ASC-US HPV16-positivo ou atipias em células glandulares - AGC).
A aplicação de p16, em que pese o seu alto valor preditivo negativo, possui valor considerado como limitado em predizer a evolução ou estratificar o risco de pacientes portadoras de NIC 1, não devendo alterar os protocolos de conduta atualmente recomendados.
Já a utilização de p16 em amostras com interpretação diagnóstica de NIC 2 está associada a “redução do grau” (isto é, para LIEBG) em até cerca de um terço dos casos, potencialmente reduzindo a frequência de procedimentos excisionais desnecessários em pacientes sem prole constituída portadoras de lesões de menor risco biológico.
Contudo, é importante lembrar que alguns casos de LIEAG podem ser exibir resultados negativos ou duvidosos, que a especificidade do marcador p16 também não é de 100%, e que a interpretação é dificultada em amostras diminutas, cortes histológicos tangenciais ou não devidamente orientados.
Autor:
Gustavo Rubino de Azevedo Focchi
Professor adjunto do departamento de patologia da escola paulista de medicina - UNIFESP
Fonte:
Obstet Gynecol 2012;120:1465–71
DOI: http://10.1097/AOG.0b013e31827001d5
Alan G. Waxman, MD, MPH, David Chelmow, MD, Teresa M. Darragh, MD, Herschel Lawson, MD,
and Anna-Barbara Moscicki, MD
A infecção HPV na gestação.
As adaptações do organismo materno à gravidez têm como objetivo principal preparar a mulher para a gestação e o parto. Dentre estas adaptações, as mudanças hormonais promovem alterações no epitélio e nos tecidos subepiteliais cervicais visando preparar o colo uterino para o parto.
Durante o trabalho de parto a cérvice aumenta 10 vezes o seu diâmetro sendo considerável a habilidade de se submeter a modificações de tamanha importância em espaço de tempo relativamente pequeno.
No epitélio estratificado escamoso observa-se hiperatividade na camada das células basais e proliferação da camada de células intermediárias. O epitélio cilíndrico sofre hipertrofia, hiperplasia e metaplasia. Também se observa modificações no estroma do colo uterino com grande aumento de vasos sanguíneos e edema.
A decidualização ou deciduose ocorre nos epitélios cervicais e também no estroma que passa a apresentar as modificações semelhantes às observadas no endométrio gravídico. Ao exame macroscópico o colo encontra-se hipertrofiado, congesto e cianótico.
O exame colposcópico pode monitorizar as modificações gravídicas do epitélio cervical, porém as modificações nos tecidos subepiteliais (músculo liso, componentes celulares, fibras e matriz gelatinosa e substância fundamental) apresentam maiores dificuldades de avaliação.
1) Mecanismos fisiológicos observados no colo uterino durante a gravidez
1.1) Abertura do orifício externo sem procidência da mucosa endocervical (gapping)
1.2) Eversão que consiste na exposição do epitélio cilíndrico na ectocérvice
1.3) Metaplasia escamosa decorrente da exposição do epitélio cilíndrico ao pH vaginal ácido
A frequência e extensão destas modificações dependem principalmente da paridade. Observa-se a eversão e metaplasia escamosa com maior frequência nas primigestas enquanto a abertura do orifício externo é mais comum nas multíparas.
2) Exame citológico durante a gravidez
Embora a gravidez não seja o momento ideal para realizar o rastreamento do câncer do colo do útero, talvez seja a única oportunidade de diagnosticar uma lesão precursora ou um carcinoma cervical inicial. Portanto, o rastreamento do carcinoma do colo uterino pode fazer parte dos exames de rotina da assistência pré-natal, desde que a grávida se enquadre dentre os critérios de população alvo para o rastreio de lesões precursoras e câncer do colo do útero.
O carcinoma do colo uterino é a neoplasia mais frequente durante a gestação e a colpocitologia é eficaz em detectar as lesões precursoras e invasoras da cérvice uterina.
O exame colpocitológico realizado durante a gestação pode apresentar dificuldades na interpretação sendo fundamental que o obstetra informe ao citopatologista a idade gestacional. Em geral, a gravidez não modifica significativamente os índices de falso-negativos deste exame.
As gestantes que apresentam exame colpocitológico alterado serão conduzidas como se não estivessem grávidas, ou seja, as atipias citológicas como células atípicas de significado indeterminado que não excluem lesão de alto grau (ASCH), lesão intraepitelial de alto grau, lesão de alto grau que não exclui invasão, o carcinoma micro ou francamente invasor, o adenocarcinoma in situ ou invasor e outras neoplasias devem ser avaliadas pela colposcopia.
3) Colposcopia/Genitoscopia durante a gravidez
Devido às alterações fisiológicas próprias da gravidez anteriormente relatadas, a avaliação colposcópica pode apresentar dificuldades principalmente a partir do 2º trimestre quando o aumento da cérvice, o muco cervical espesso e o prolapso das paredes vaginais dificultam a visualização do colo. Entretanto, pela eversão fisiológica da gravidez a junção escamocolunar (JEC) costuma ser de fácil visualização e avaliação principalmente após a 12ª semana de gestação.
Além disto, algumas mudanças benignas podem simular lesões graves e devido ao grande aumento da vascularização um pequeno foco de carcinoma pode não ser diagnosticado, sendo importante examinador experiente.
A principal indicação da colposcopia é a atipia citológica detectada no exame colpocitológico e, em gestantes, a biópsia dirigida está indicada quando a colposcopia é sugestiva de invasão.
A biópsia dirigida pela colposcopia constitui método seguro e confiável na avaliação de gestantes com colpocitologia e colposcopia alteradas, sendo fundamental para descartar carcinoma invasor.
Vários instrumentos podem ser utilizados para este fim como a pinça de Medina modificada, com risco mínimo de hemorragia devido ao pequeno tamanho do fragmento. A escolha do instrumental dependerá da experiência e preferência do colposcopista e da disponibilidade de cada serviço.
4) Neoplasias intraepiteliais cervicais (NIC) ou Lesões intraepiteliais (LIE) na gravidez
O evento fisiológico da eversão no colo uterino estimula o desenvolvimento de metaplasia escamosa caracterizando a Zona de Transformação (ZT). As células metaplásicas apresentam alto metabolismo e são as preferencialmente infectadas pelo HPV. A partir desta infecção, porém na dependência de inúmeros fatores entre estes o sistema imunológico, poderá se observar atipias na ZT (ZT Atípica).
A infecção pelo HPV é atualmente a infecção viral de transmissão sexual mais frequente em todo o mundo com elevada prevalência no período de vida reprodutiva. Portanto, é esperado que a prevalência desta infecção também seja elevada na gravidez.
Há de se considerar também as modificações fisiológicas do sistema imunológico durante este período como a diminuição do número e atividade dos linfócitos TCD4 e das imunoglobulinas das classes G e A no muco cervical e diminuição da síntese de mácrofagos devido aos altos níveis de hormônios esteróides.
Todas estas modificações facilitam a proliferação do HPV, proporcionando lesões mais extensas e volumosas durante a gravidez. Vários trabalhos têm avaliado a história natural das NIC/LIE durante a gravidez e não observaram maior risco de progressão histológica para carcinoma invasor.
A presença de NIC/LIE independente do grau, não constitui contraindicação para o parto vaginal sendo a cesárea indicada por critérios puramente obstétricos.
Em 1988, Adhoot e colaboradores avaliando esfregaços cervicais realizados no puerpério descreveram um aumento nas taxas de regressão das lesões intraepiteliais de alto grau (LIEAG/NIC II e III) em mulheres que tiveram suas gestações resolvidas por parto vaginal quando comparadas com as pacientes submetidas à cesárea (48% de regressão em 59 mulheres que tiveram parto vaginal Versus 0% de regressão em 12 pacientes que tiveram cesárea).
Para Yost et al, 1999 não houve diferença nas taxas de regressão das NIC II e III em relação ao tipo de parto, embora estas taxas tenham sido elevadas (68% regressão para NIC II e 70% de regressão para NIC III).
Após correta avaliação do tripé diagnóstico (colpocitologia, genitoscopia e anátomo-patológico) confirmando a presença de NIC/LIE de alto ou baixo grau, excluindo-se a invasão, é consenso que durante a gestação seja realizado acompanhamento com colpocitologia e colposcopia a cada 8 ou 12 semanas. O tratamento excisional deve ser postergado para o período pós-parto.
O momento ideal para repetição da propedêutica seria após o retorno aos ciclos menstruais, porém na prática realiza-se esta reavaliação com 8 a 12 semanas pós-parto. A taxa de regressão da NIC não tratada na gravidez varia de 25 a 70%.
A genitoscoscopia realizada por examinador experiente associada à biópsia dirigida tem elevada sensibilidade para diagnosticar doença invasora do colo e a conização tem indicações limitadas durante a gestação, sendo reservada aos casos em que a biópsia dirigida evidenciar microinvasão ou invasão.
Recomenda-se realizá-la no 2º trimestre com objetivo de diferenciar as pacientes que podem esperar até o termo da gestação para tratar a doença e aquelas que o tratamento deve ser imediato, sempre considerando o desejo materno.
É importante ressaltar que a ocorrência de complicações como hemorragias e alta frequência de margens comprometidas pela neoplasia em qualquer técnica empregada para conização não permitem que este procedimento seja considerado terapêutico para as LIEAG/NICII e III durante a gestação.
Referências consultadas:
Jamieson, DJ; Theiler, RN; Rasmussen, SA. Emerging infections and pregnancy.
Emerg Infect Dis, [S.1], v. 12, n. 11, p. 1638-43, nov. 2006.
Kaplan KJ, Dainty LA, Dolinsky B, Rose GS, Carlson J, McHale M, Elkans JC. Prognosis and recurrence risk for patients with cervical squamous intraepithelial lesions diagnosed during pregnancy. (2004) American Cancer Society
Massad SL, Wright TC, Cox TJ, Twiggs LB, Wilkinson E. Managing abnormal cytology results in pregnancy. J Low Genit Tract Dis. 2005;9:146-148.
Nobbenhuis MAE, Helmerhorst TJM, van den Brule AJC, Rozendaal L, Bezemer PD, Voorhorst FJ and Meijer CJLM. High-risk human papillomavirus clearance in pregnant women: trends for lower clearance during pregnancy with a catch-up postpartum.
British Journal of Cancer (2002) 87, 75 –80
Siddiq, TS, Twigg, JP, Hammond, RH. Assessing the accuracy of colposcopy at predicting the outcome of abnormal cytology in pregnancy. European Journal of Obstetrics,Gynecology and Reproductive Biology 2006, 124(1), 93–97.
Yamakazi T, Inaba F, Takeda N, Furuno M, Kamemori T, Kosaka N, Ohta Y, Fukasawa I, Inaba N. A study ao abnormal cervical cytology in pregnant women. (2005) Arch Gynecol Obstet 273: 355-359.
INCA, 2016. Diretrizes para o rastreamento do Cancer cervical
Autora:
Silvana Quintana, Professora Associada do Departamento de Ginecologia e Obstetrícia da Faculdade de Medicina de Ribeirão Preto - Universidade de São Paulo-FMRPUSP, Brasil
Preservação da fertilidade em mulheres com câncer.
A capacidade de começar uma família e ter filhos é uma questão chave na qualidade de vida. A infertilidade após tratamento do câncer tem um reconhecido impacto negativo nessa qualidade de sobrevivência.
A incidência do câncer continua a crescer mundialmente devido ao aumento da expectativa de vida da população e de hábitos de vida associados às malignidades como o tabagismo. Nas últimas duas décadas a sobrevida dos pacientes com câncer aumentou substancialmente. Dessa forma, houve um maior interesse na qualidade de vida dos sobreviventes, incluindo a possibilidade de preservação do futuro reprodutivo.
O principal objetivo do tratamento oncológico é a cura, que muitas vezes se baseia na cirurgia, quimioterapia e radioterapia. No entanto, esses procedimentos podem resultar em um comprometimento total ou parcial da fertilidade. As taxas de infertilidade após um tratamento oncológico dependem de vários fatores.
Os efeitos da quimioterapia dependem da droga utilizada, método de administração, idade da paciente e tratamento prévio para infertilidade. Uma cirurgia mais conservadora que possa permitir a preservação do futuro reprodutivo pode ser uma opção em casos selecionados. Novas técnicas como a maturação in vitro de folículos e o transplante de tecido ovariano constituem perspectivas para essas mulheres.
Técnicas de reprodução assistida para da fertilidade
As técnicas de reprodução assistidas aplicadas às pacientes com câncer de ovário, como a criopreservação de oócitos, tecido ovariano ou mesmo embriões não são tão comuns, por isso as dificuldades em analisar dados sobre o assunto.
Na criopreservação de tecido ovariano, uma técnica ainda considerada de caráter experimental, existe a preocupação de adicionar o risco de inoculação de células do tumor. Sua indicação em mulheres com câncer de ovário é controversa. Há necessidade de uma estreita colaboração entre clínicas oncológicas e centros de reprodução nestes casos, o que pode ser vantajoso para garantir a saúde reprodutiva das mulheres.
Outra consideração importante diz respeito às pacientes que vão precisar de tratamento adjuvante. É sabido que a quimioterapia consistentemente compromete a função ovariana, muitas vezes resultando em infertilidade e menopausa precoce, dependendo das diferentes drogas e esquemas. A decisão quanto à necessidade de terapia adjuvante deve ser realizada independentemente da cirurgia realizada (radical ou conservadora), a fim de não comprometer o resultado oncológico.
Os estudos investigando os efeitos da supressão ovariana nos marcadores da reserva de oócitos atualmente não suportam o uso do análogo de GnRH como uma estratégia eficaz na tentativa de preservar a função ovariana e a fertilidade feminina durante tratamentos de quimioterapia.
As mulheres adultas que desejam preservar a fertilidade podem ser submetidas a estimulação controlada da ovulação com indutores para recuperação de oócitos maduros e congelamento, ou se desejarem, para fertilização in vitro (FIV) e congelamento de embriões.
Geralmente a estimulação ovariana controlada por medicação para fertilização in vitro pode exigir entre 2 a 6 semanas, dependendo da fase do ciclo menstrual que a paciente estiver quando do planejamento e início do tratamento. Nos casos onde o tratamento oncológico deverá começar dentro de 3 a 4 semanas e não é desejável aguardar a próxima menstruação para iniciar um protocolo de estimulação, têm sido propostos protocolos de início aleatório. Assim essas pacientes podem completar um ciclo de estimulação para preservação da fertilidade dentro de duas semanas e iniciar o tratamento de câncer conforme planejado.
Outras opções que podem ser consideradas, apesar de experimentais até o momento incluem: a combinação de recuperação de oócitos imaturos seguida de maturação in vitro (MIV) e vitrificação de oócitos e a combinação de tecido ovariano congelado com descongelamento e posterior recuperação dos oócitos imaturos seguido por MIV e vitrificação desses oócitos, desde que essas técnicas podem levar a possibilidade de nascidos vivos.
Outra alternativa, também considerada uma técnica experimental, seria a cultura in vitro de folículos em estágios iniciais com o objetivo de desenvolvê-los em competentes folículos maduros, isolados de um pedaço de tecido ovariano descongelado. Talvez essa será a opção futura para pacientes com malignidades hematológicas e de ovário na tentativa de minimizar os riscos de proliferação de células malignas em pacientes já tratados para a enfermidade oncológica.
O ciclo natural de fertilização in vitro (sem estimulação hormonal) ou indução de ovulação usando protocolos alternativos e potencialmente seguros, incluindo o uso moduladores seletivos de receptores de estrogênio (SERMs) e inibidores da aromatase, sozinhos ou em combinação com gonadotrofinas têm sido propostos.
As desvantagens do ciclo natural seriam o fato de obter-se apenas um oócito ou embrião por tentativa e a alta taxa de cancelamento por ciclo. Protocolos de estimulação usando letrozole associados a gonadotrofinas são atualmente preferidos sobre protocolos de tamoxifeno.
O tratamento com letrozol mostrou ser mais eficaz e está associado a um maior número de oócitos obtidos e fertilizados quando comparado ao tamoxifeno. O seguimento a curto prazo de pacientes com câncer da mama submetidos a estimulação ovariana com letrozol para preservação de fertilidade não demonstrou efeitos prejudiciais nos desfechos dos ciclos de tratamento.
A maturação do oócito com agonistas de GnRH (GnRHa) no lugar do uso da gonadotrofina coriônica humana (hCG) tem conseguido diminuir a exposição ao estradiol, reduzindo concomitantemente o risco de síndrome de hiperestimulação ovariana, uma complicação conhecida da estimulação ovariana controlada.
Embora os inibidores de aromatase sejam contra-indicados durante a gravidez, dados indicam que os tratamentos de fertilidade com letrozol não induzem qualquer aumento de riscos para o feto.
Quanto ao congelamento de oócitos, as taxas de fertilização e gravidez são semelhantes à fertilização in vitro utilizando oócitos frescos e não foi observado nenhum aumento em anormalidades cromossômicas, defeitos congênitos ou défices do desenvolvimento em crianças nascidas de oócitos criopreservados. Tornou-se uma técnica segura e viável para preservação de gametas e possibilidade de manter a fertilidade futura.
Autor:
Rívia Mara Lamaita
CNE Reprodução Humana
O selo de qualidade da mamografia.
Você às vezes tem a impressão de que a mamografia que solicita para as suas pacientes pode não ter a qualidade ideal? Quer saber como atestar a qualidade de uma mamografia?
Bem existem ferramentas poderosas para fazer essa aferição, por exemplo apuração da sensibilidade, especificidade e taxa de detecção. Infelizmente, o levantamento desses dados é trabalhoso e caro, e quase não é feito por nenhum serviço no Brasil, embora seja obrigatório em outros países.
Mas o Brasil não é de todo desprovido de iniciativas para promover a qualidade da mamografia. Há muitos anos três sociedades se uniram para realizar essa tarefa: a Febrasgo, o Colégio Brasileiro de Radiologia e a Sociedade Brasileira de Mastologia. Foi criada uma comissão que se reúne uma vez por mês para analisar serviços de mamografia, além de cuidar de vários outros assuntos pertinentes ao tema, que recebeu o nome de Comissão Nacional de Mamografia.
A comissão avalia os serviços que, se aprovados, recebem o Certificado de Qualidade em Mamografia, passando a ter o direito de exibir nos seus documentos (inclusive laudos) o Selo de Qualidade em Mamografia.
Os selos são outorgados por aparelho de mamografia. Se uma clínica tiver mais de um aparelho, cada um deles deverá ser avaliado separadamente. São analisados os dados físicos radiométricos (dose de radiação, laudo de proteção das salas e outros parâmetros técnicos). Em seguida, são avaliados cinco exames realizados naquele aparelho. A avaliação leva em conta a qualidade das radiografias, posicionamento, presença de artefatos, identificação de lesões, descrição dos achados e conduta recomendada.
Se você se importa que a sua paciente faça uma mamografia de qualidade, procure saber se o serviço de mamografia para onde você encaminha suas pacientes tem o selo de qualidade. É a melhor iniciativa dentro do Brasil para incrementar a qualidade da mamografia.
O que o selo não mede? Justamente os parâmetros de auditoria dita de resultados mencionados acima (sensibilidade, especificidade e taxa de detecção). Infelizmente, pois eles são a verdadeira “prova dos nove” da qualidade da mamografia. Mas você pode usar de uma “auditoria cotidiana” para avaliar qualidade da mamografia.
Todos os falsos negativos devem ser analisados a fundo. A definição de falso negativo é o aparecimento de um câncer de mama até um ano após um exame. Como a mamografia não detecta todos os cânceres, um falso negativo não significa necessariamente um erro, mas se um serviço tiver muitos falsos negativos, ou se a radiografia lida como negativa mostrar retrospectivamente uma lesão suspeita óbvia, considerar que esse serviço possa ter baixa sensibilidade e taxa de detecção abaixo do aceitável.
As recomendações de biópsia, por sua vez, darão uma ideia da especificidade. Em geral a cada dez recomendações de biópsia, três a quatro deverão resultar em câncer. Um serviço que tenha um número muito grande de biópsias benignas levanta a suspeita de estar indicando mal essas biópsias (baixa especificidade).
Talvez pior do que não fazer mamografia seja fazer uma mamografia malfeita, que pode resultar em radiação acima do aceitável, biópsias desnecessárias, reconvocações e recomendações de exames complementares exageradas, custos aumentados, e até mesmo falsa segurança no caso de um exame falso negativo com retardo no diagnóstico e no tratamento.
É fundamental, portanto, zelarmos pela qualidade da mamografia. A ferramenta já consolidada no Brasil é o selo de qualidade. As ferramentas de auditoria de resultados não são usadas em larga escala no Brasil, mas pode-se usar uma “auditoria cotidiana” para aferir a qualidade da mamografia.
A exigência de qualidade deve, antes de tudo, ser um estímulo para os serviços que fazem a mamografia se aperfeiçoem cada vez mais, se reciclem, atualizem seus aparelhos e seus processos. Seja chato, exija qualidade. A sua paciente agradece.
Autor:
Hélio Sebastião Amâncio de Camargo Júnior