Realizações Diretoria NOVA FEBRASGO
O mundo digital trouxe uma serie de possibilidades para a democratização da informação, no sentido de tornar o acesso a conteúdo mais atrativo e moderno. Com o apoio dos colaboradores e da comunidade científica, a FEBRASGO está caminhando para o nova roupagem, uma abordagem mais próxima dos associados e de todos que fazem parte desta luta: promover saúde e cuidados para todas as mulheres do Brasil.
Faça o download no nosso book de realizações e conheça todos os projetos da FEBRASGO.
IGCS 2019 - A REUNIÃO GLOBAL ANUAL DA SOCIEDADE INTERNACIONAL DO CÂNCER GINECOLÓGICO
CONHEÇA O IGCS
O EVENTO
No Encontro Global, o IGCS se uniu a sociedades nacionais e regionais, como a FEBRASGO, para oferecer um programa abrangente que abrange as mais recentes informações de ponta, incluindo desenvolvimentos inovadores em cirurgia, quimioterapia, radioterapia e patologia. Esta reunião é multidisciplinar e baseia-se em conhecimentos de todo o mundo. 2019 será a primeira reunião anual do IGCS e, com esta alteração, inclui o objetivo, tal como definido pelo Conselho do IGCS, de continuar a internacionalizar a reunião e reestruturar o Comité do Programa Científico. Presidentes regionais das principais áreas do mundo foram designados e esses presidentes criaram comitês em sua região.
Este comitê verdadeiramente internacional de especialistas de classe mundial em oncologia ginecológica está desenvolvendo um programa científico que cobrirá uma ampla gama de tópicos. Vamos nos concentrar em apresentar palestras de última geração e pesquisas sobre tópicos relevantes de todo o mundo, que proporcionarão sessões interativas e a oportunidade de trocar idéias. Tópicos relacionados a problemas de renda baixa e média serão abordados extensivamente, incluindo desafios educacionais e melhor utilização de recursos limitados.
O Rio de Janeiro, ou simplesmente o Rio, é uma das cidades mais bonitas da América do Sul. A sua natureza deslumbrante e a combinação única de paisagem montanhosa e belíssima frente de praia fazem desta cidade verdadeiramente única. Não é de surpreender que parte do Rio seja protegida pela UNESCO como Patrimônio da Humanidade. O cenário de tirar o fôlego e a beleza natural não são as únicas experiências que a cidade tem a oferecer. O samba dinâmico, a bossa nova melódica, os museus e a calorosa hospitalidade dos habitantes locais são o que torna inesquecível a experiência nesta jóia brasileira de uma cidade.
Inscreva-se clicando aqui.
REPRODUÇÃO: Site IGCS 2019
Leia uma prévia dos Protocolos Assistênciais da FEBRASGO
A FEBRASGO disponibilizou uma prévia de dois protocolos assistências para leitura. Clique nos links abaixo para ter acesso.
OMS define 10 prioridades de saúde para 2019
A Organização Mundial da Saúde (OMS) tem metas ambiciosas para 2019. Entre os objetivos da agência da ONU, está a ampliação do acesso e da cobertura de saúde para atender a 1 bilhão a mais de pessoas na comparação com números atuais. A instituição também quer garantir que 1 bilhão de indivíduos estejam protegidos de emergências de saúde. Para tirar essas resoluções do papel, a OMS estipulou dez prioridades para o ano que se inicia.
A Organização Mundial da Saúde (OMS) tem metas ambiciosas para 2019. Entre os objetivos da agência da ONU, está a ampliação do acesso e da cobertura de saúde para atender a 1 bilhão a mais de pessoas na comparação com números atuais. A instituição também quer garantir que 1 bilhão de indivíduos estejam protegidos de emergências de saúde. Por fim, o organismo espera melhorar o bem-estar de 1 bilhão de moradores do planeta Terra. Mas como cumprir essa agenda em um ano?
Para tirar essas resoluções do papel, a OMS estipulou dez prioridades para o ano que se inicia. A lista inclui o combate à poluição ambiental e às mudanças climáticas, infecções transmissíveis como o ebola, a dengue, a gripe e o HIV, doenças crônicas e outros desafios de saúde pública. Confira abaixo e entenda por que esses temas serão críticos em 2019:
1. Poluição do ar e mudanças climáticas

Trânsito em viaduto de Beijing, na China. Foto: Banco Mundial/Li Lou
Nove em cada dez pessoas respiram ar poluído todos os dias. Em 2019, a poluição do ar é considerada pela OMS como o maior risco ambiental para a saúde. Poluentes microscópicos podem penetrar nos sistemas respiratório e circulatório de uma pessoa, danificando seus pulmões, coração e cérebro. Isso resulta na morte prematura de 7 milhões de pessoas todos os anos, devido a enfermidades como câncer, acidente vascular cerebral e doenças cardiovasculares e pulmonares. Cerca de 90% dessas mortes ocorrem em países de baixa e média renda, com altos volumes de emissões da indústria, dos transportes e da agricultura, além do cozimento por meio de combustíveis ou tecnologias poluentes em ambientes interiores.
A principal causa da poluição do ar — a queima de combustíveis fósseis — também é um dos principais fatores que contribuem para a mudança climática, a qual afeta a saúde das pessoas de diferentes maneiras. Entre 2030 e 2050, espera-se que as mudanças climáticas causem 250 mil mortes a mais por ano devido à desnutrição, malária, diarreia e estresse por calor.
Em outubro de 2018, a OMS realizou sua primeira Conferência Global sobre Poluição do Ar e Saúde, em Genebra. Países e organizações firmaram mais de 70 compromissos para melhorar a qualidade do ar. Neste ano, a Cúpula do Clima da Organização das Nações Unidas ocorrerá em setembro e tem como objetivo fortalecer a ação climática e seus esforços em todo o mundo. Mesmo que todos os compromissos assumidos pelos países junto ao Acordo de Paris sejam alcançados, o mundo ainda está em vias de se aquecer por mais de 3°C até o final deste século.
2. Doenças crônicas não transmissíveis
Dietas poucos saudáveis são algumas das causas das doenças crônicas não transmissíveis. Foto: PEXELS (CC)/Robin Stickel
As doenças crônicas não transmissíveis – como diabetes, câncer e doenças cardiovasculares – são responsáveis por mais de 70% de todas as mortes no mundo — o equivalente a 41 milhões de falecimentos. Isso inclui 15 milhões de pessoas que morrem prematuramente, ou seja, com idade entre 30 e 69 anos. Mais de 85% dessas mortes precoces ocorrem em países de baixa e média renda. O aumento da ocorrência dessas doenças tem sido impulsionado por cinco fatores de risco: o uso do tabaco, a inatividade física, o uso nocivo do álcool, as dietas pouco saudáveis e a poluição do ar. Esses fatores também agravam problemas de saúde mental, que podem se originar desde cedo. Metade de todos os transtornos mentais começa aos 14 anos, mas a maioria dos casos não é detectada e tratada de forma oportuna. O suicídio, por exemplo, é a segunda causa de morte entre adolescentes de 15 a 19 anos. Em 2019, a OMS trabalhará com os governos para atingir a meta global de redução em 15% da inatividade física até 2030. Isso será feito por meio de ações como a implementação da ACTIVE, uma série de políticas que incentivam as pessoas a estar mais ativas todos os dias.
3. Pandemia de gripe
Profissional de saúde animal monitora presença de vírus da gripe aviária na Indonésia. Foto: FAO/Sadewa Sadewa
O mundo enfrentará outra pandemia de influenza – o que ainda não se sabe é quando ela chegará e o quão grave será. A OMS está constantemente monitorando a circulação dos vírus influenza para detectar possíveis cepas pandêmicas: 153 instituições em 114 países estão envolvidas na vigilância e resposta global. Todos os anos, a OMS recomenda quais cepas devem ser incluídas na vacina contra a influenza para proteger as pessoas da gripe sazonal. No caso de uma nova cepa desenvolver um potencial pandêmico, a agência da ONU possui uma grande parceria com os principais atores na área, a fim de garantir acesso efetivo e equitativo a diagnósticos, vacinas e tratamentos antivirais, especialmente em países em desenvolvimento.
4. Cenários de fragilidade e vulnerabilidade
Para fugir da violência, famílias sírias montam acampamento improvisado ao norte de Idlib. Imagem de setembro de 2018. Foto: UNICEF/Watad
Mais de 1,6 bilhão de pessoas — 22% da população mundial — vivem em locais onde crises prolongadas (uma combinação de fatores como seca, fome, conflitos e deslocamento populacional) e serviços de saúde mais frágeis as deixam sem acesso aos cuidados básicos de que necessitam. Existem cenários frágeis em quase todas as regiões do mundo. Nesses contextos, a metade das principais metas de desenvolvimento sustentável, incluindo sobre saúde infantil e materna, permanece não atendida. A OMS continuará trabalhando com esses países para fortalecer os sistemas de saúde, de modo a prepará-los para detectar e responder a surtos de doenças. O organismo também quer tornar essas nações capazes de prestar serviços de saúde de alta qualidade, incluindo os de vacinação.
5. Resistência antimicrobiana
Consumo excessivo e inadequado de antibióticos aumenta a resistência de bactérias a esses medicamentos. Foto: PEXELS
O desenvolvimento de antibióticos, antivirais e antimaláricos são alguns dos maiores êxitos da medicina moderna. Agora, a eficácia de algumas dessas drogas está acabando. A resistência antimicrobiana – a capacidade de bactérias, parasitas, vírus e fungos resistirem a esses medicamentos – ameaça nos mandar de volta a uma época em que não conseguíamos tratar facilmente infecções como pneumonia, tuberculose, gonorreia e salmonelose. A incapacidade de prevenir infecções pode comprometer seriamente cirurgias e procedimentos como a quimioterapia. A resistência aos medicamentos contra a tuberculose é um grande obstáculo para combater uma enfermidade que acomete cerca de 10 milhões de pessoas e mata 1,6 milhão delas todos os anos. Em 2017, cerca de 600 mil casos de tuberculose foram diagnosticados como resistentes à rifampicina – droga de primeira linha mais eficaz – e 82% dessas pessoas apresentavam tuberculose multirresistente. A resistência aos medicamentos é impulsionada pelo uso excessivo de remédios antimicrobianos em pessoas, mas também em animais, especialmente os que são utilizados na produção de alimentos e no meio ambiente. A OMS trabalha com esses setores para implementar um plano de ação global de combate à resistência antimicrobiana, aumentando a conscientização e o conhecimento sobre o tema, reduzindo as infecções e incentivando a aplicação adequada desses medicamentos.
6. Ebola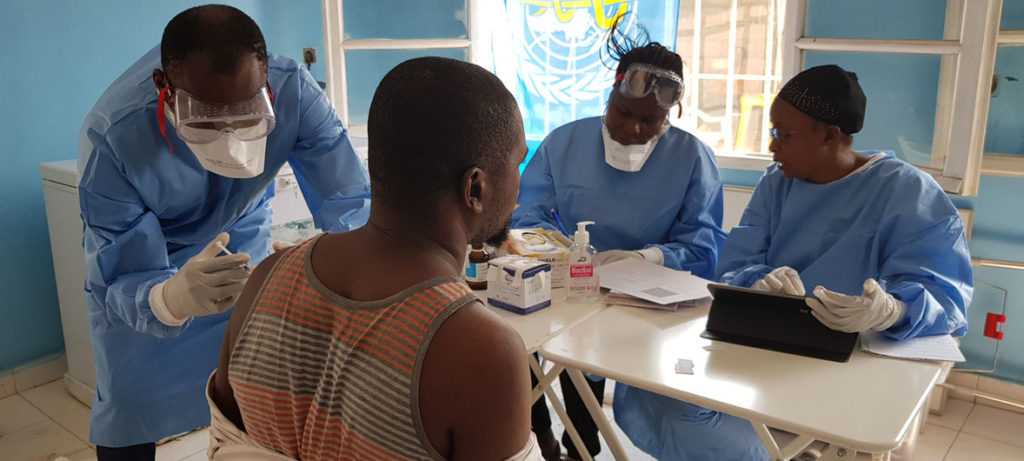
Médico vacina profissional de saúde na cidade de Mbandaka, na República Democrática do Congo, em junho de 2018. Foto: OMS/Lindsay Mackenzie
Em 2018, a República Democrática do Congo foi palco de dois surtos de ebola, que se espalharam para cidades com mais de 1 milhão de pessoas. Uma das províncias afetadas também está em zona de conflito. Isso mostra que o contexto é crítico, quando se trata de um agente patogênico que ameaça a saúde global, como é o caso do ebola. O que aconteceu em surtos em áreas rurais no passado nem sempre vale para as zonas urbanas densamente povoadas ou para locais afetados por conflitos. Em uma conferência sobre a preparação para emergências, realizada em dezembro de 2018, participantes dos setores de saúde pública, saúde animal, transporte e turismo discutiram os desafios crescentes no combate de surtos em regiões urbanas. Eles pediram à OMS e seus parceiros que considerem 2019 como um ano de ações de preparação para situações de emergência. O plano R&D Blueprint da OMS identifica doenças e patógenos com potencial de causar uma emergência de saúde pública, mas que carecem de tratamentos e vacinas eficazes. Esta lista de pesquisa e desenvolvimento prioritários inclui o ebola, febres hemorrágicas, o vírus zika, o vírus Nipah, a síndrome respiratória por coronavírus do Oriente Médio, a síndrome respiratória aguda grave e a “doença X” – esse último item representa a necessidade de se preparar para um agente patogênico desconhecido, que poderia provocar uma grave epidemia.
7. Atenção primária de saúde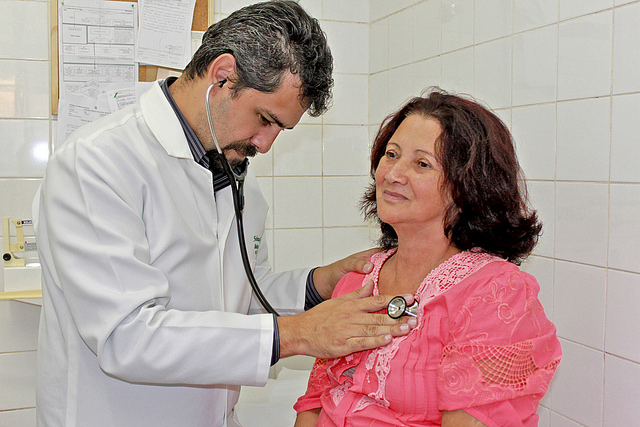
Sistemas de saúde baseados numa atenção primária forte são fundamentais para garantir a cobertura universal de saúde. Foto: Flickr/Portal PBH
A atenção primária de saúde é geralmente o primeiro ponto de contato que as pessoas têm com o seu sistema de saúde e, idealmente, deve fornecer, ao longo da vida, cuidados integrados, acessíveis e baseados na comunidade. Os cuidados de saúde primários podem atender à maioria das necessidades de saúde de uma pessoa ao longo da sua vida. Sistemas de saúde com uma atenção primária forte são necessários para se alcançar a cobertura universal de saúde. No entanto, muitos países não têm instalações de atenção primária de saúde adequadas. Em outubro de 2018, a OMS co-organizou uma importante conferência global em Astana, no Cazaquistão, onde todos os países renovaram seu compromisso com a atenção primária de saúde. Esse posicionamento já havia sido oficializado na Declaração de Alma-Ata, em 1978. Em 2019, a OMS trabalhará com parceiros para revitalizar e fortalecer a atenção primária de saúde nos países e dar seguimento aos compromissos específicos assumidos na Declaração de Astana.
8. Relutância em vacinar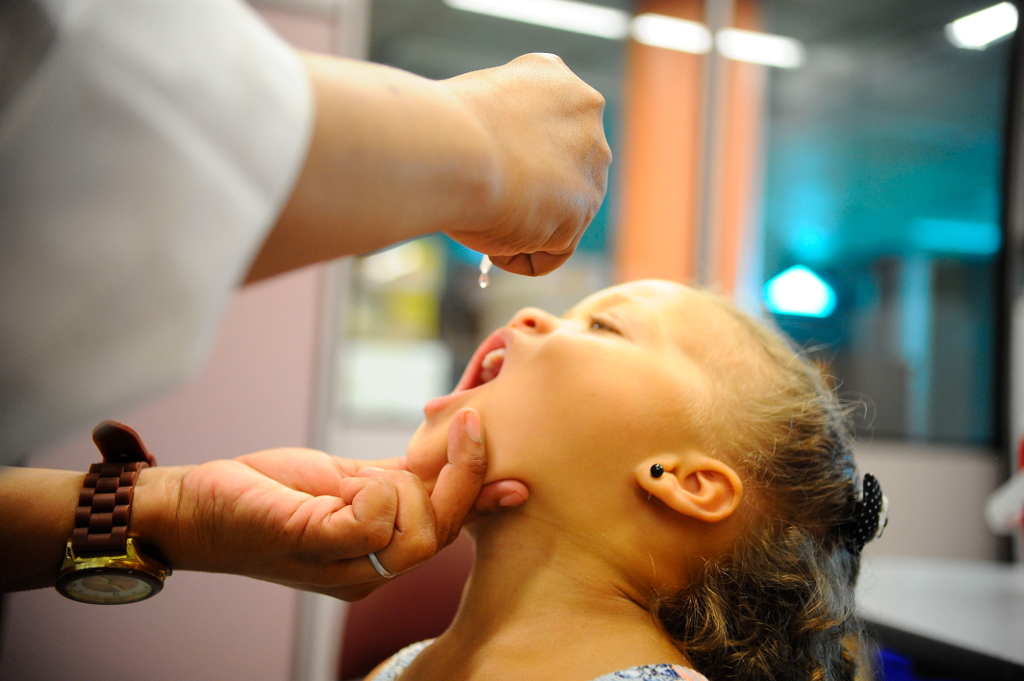
Campanha de vacinação contra a pólio no Brasil. Foto: Tomaz Silva/Agência Brasil
A hesitação para vacinar – a relutância ou a recusa, apesar da disponibilidade da vacina – ameaça reverter o progresso feito no combate a doenças que podem ser prevenidas por meio da imunização. Trata-se de uma das formas mais custo-efetivas para evitar doenças e fatalidades. Atualmente, previnem-se cerca de 2 a 3 milhões de mortes por ano. Outras 1,5 milhão de mortes poderiam ser evitadas se a cobertura global de vacinação tivesse maior alcance. O sarampo, por exemplo, registrou um aumento de 30% nos casos em todo o mundo. As razões para esse crescimento são complexas e nem todos os casos se devem à chamada hesitação vacinal. No entanto, alguns países que estavam perto de eliminar a doença testemunharam seu ressurgimento. As razões pelas quais as pessoas escolhem não se vacinar são complexas. Um grupo consultivo de vacinas para a OMS identificou a “complacência”, a “inconveniência” no acesso às vacinas e a falta de confiança como os principais motivos dessa relutância. Os profissionais de saúde, especialmente os que fazem parte das comunidades, continuam sendo os conselheiros e influenciadores mais confiáveis nas decisões sobre vacinação. Segundo a OMS, eles devem ser apoiados para fornecer informações de credibilidade sobre as vacinas. Em 2019, a OMS intensificará os esforços para eliminar o câncer do colo de útero em todo o mundo, aumentando a cobertura da vacina contra o HPV, entre outras medidas. Esse também pode ser o ano em que a transmissão do poliovírus selvagem seja interrompida no Afeganistão e no Paquistão. No ano passado, menos de 30 casos foram registrados nos dois países. A OMS e seus parceiros estão empenhados em apoiá-los na vacinação de todas as crianças, a fim de erradicar definitivamente a poliomielite, uma doença incapacitante.
9. Dengue
Mosquito Aedes aegypti é principal vetor do vírus da dengue, zika e chikungunya. Foto: UNICEF/BRZ/Ueslei Marcelino
A dengue é uma doença transmitida por mosquitos e pode causar sintomas semelhantes aos da gripe. Essa infecção tem sido uma crescente ameaça de saúde nas últimas décadas e pode ser letal — a enfermidade mate até 20% das pessoas que desenvolvem sua forma grave. Um grande número de casos ocorre durante as estações chuvosas de países como Bangladesh e Índia. Atualmente, no período de sazonalidade, os episódios vêm aumentando significativamente — em 2018, Bangladesh registrou o maior número de mortes pela doença em quase duas décadas. A dengue já está se espalhando para países menos tropicais e mais temperados, como o Nepal, que tradicionalmente não apresentava ocorrências da patologia em seu território. Estima-se que 40% de todo o mundo está em risco de contrair o vírus da dengue: são cerca de 390 milhões de infecções por ano. A estratégia da OMS para controlar a doença visa reduzir as mortes em 50% até 2020
10. HIV
Foto: UNAIDS
Os progressos contra o HIV têm sido enormes, com o fornecimento de remédios antirretrovirais para 22 milhões de pessoas no mundo e o acesso ampliado a métodos de prevenção, como a profilaxia pré-exposição (PrEP). Essa técnica envolve o uso de antirretrovirais para prevenir a infecção, sobretudo entre pessoas com maior risco de contrair HIV. Esforços também avançaram na conscientização sobre a importância da testagem. Apesar disso, a epidemia continua a se alastrar, com quase 1 milhão de pessoas morrendo por HIV/AIDS a cada ano. Desde o início da epidemia, mais de 70 milhões de pessoas adquiriram a infecção. Desse grupo, cerca de 35 milhões morreram. Atualmente, em torno de 37 milhões de indivíduos em todo o mundo vivem com o HIV. Alcançar pessoas como profissionais do sexo, pessoas privadas de liberdade, homens que fazem sexo com homens e pessoas transexuais é extremamente desafiador, uma vez que esses grupos são excluídos dos serviços de saúde. Uma parcela populacional cada vez mais afetada são as adolescentes e as mulheres jovens (entre 15 e 24 anos), que estão particularmente em alto risco e representam uma em cada quatro infecções por HIV na África Subsaariana, apesar de serem apenas 10% da população. Neste ano, a OMS trabalhará com os países para apoiar a introdução do autoteste, para que um número cada vez maior de pessoas que vivem com HIV conheça o seu status e possa receber tratamento ou medidas preventivas. Uma das atividades previstas será a difusão de novas orientações para empresas e organizações, a fim de apoiar essas instituições no oferecimento de autotestes de HIV nos locais de trabalho. Essas recomendações foram anunciadas em dezembro de 2018 pela OMS e pela Organização Internacional do Trabalho (OIT).
Reprodução: Site ONU Brasil
Biópsias de mama. O papel do ginecologista.
Introdução. Quem solicita biópsias de mama? Na maioria das vezes é o ginecologista. Em alguns locais a paciente é encaminhada ao mastologista antes de uma solicitação de biópsia e em outros locais um generalista da rede básica de saúde é quem faz essa solicitação. Para uma boa indicação é preciso conhecer diversos aspectos como: tipo de lesão, características da paciente e formas de realizar colheita tecidual e de guiar essa colheita.
Preceitos básicos. Usar o método menos invasivo e mais barato (em geral essas qualidades andam juntas) que atenda à necessidade do caso e que esteja disponível na comunidade. Preferir técnicas percutâneas (não cirúrgicas). Saber avaliar a concordância entre a suspeita imaginológica e o resultado anatomopatológico. Biopsiar apenas quem precisa de biópsia. Considero desnecessário explicar as afirmativas acima, pois todas elas são acima de tudo imperativos éticos. Vale mencionar que, caso uma forma de biópsia menos invasiva que atenda melhor à necessidade do caso não esteja disponível na comunidade, é boa norma informar à paciente para que ela decida se há conveniência em se deslocar para outro centro onde possa receber a forma de biópsia ideal.
Quando é necessário biopsiar: Lesões BI-RADS® 4 e 5, sempre. Lesões BI-RADS® 2, nunca. Lesões BI-RADS® 3, raramente. Um motivo para indicar biópsia no BI-RADS® 3 pode ser a impossibilidade de acompanhamento, como longas viagens para lugares sem assistência ou iminência de uma cirurgia mamária que possa dificultar o encontro da lesão posteriormente. Em pacientes de risco muito alto, ocasionalmente pode ser indicado biópsia de algumas lesões classificadas como BI-RADS® 3. Em lesões muito grandes no diagnóstico inicial (mais de 2 ou 2,5 cm), pode ser conveniente iniciar a abordagem com biópsia percutânea, pois em um acompanhamento semestral um eventual crescimento de um nódulo pode levá-lo a um tamanho que poderia piorar o prognóstico na eventualidade de uma condição maligna.
Tipos de pacientes. Situações particularizadas, como uma paciente com grande debilidade, podem exigir uma escolha não habitual. Portanto, as orientações abaixo não devem ser entendidas como absolutas.
Os tipos de biópsia e as formas de guiar a biópsia. As biópsias podem ser cirúrgicas ou percutâneas. As cirúrgicas estão praticamente abandonadas, mas quando for a opção, exigirá uma forma de localização pré-operatória, mesmo quando a lesão for palpável, pois há fatores durante a cirurgia que podem interferir com a identificação adequada da lesão. A localização pré-operatória pode ser feita através da colocação de um fio guia metálico ou injeção de uma substância identificável durante a cirurgia, seja um corante como carvão ou uma substância radioativa (nesse caso, além da localização da lesão, a substância radioativa por ser usada para identificar o linfonodo que drena a região de interesse na mama, chamado de linfonodo sentinela). Quando a injeção de substância radioativa tem apenas a intenção de marcar a lesão mamária, o procedimento é chamado de roll, e quando há intenção adicional de identificar o linfonodo sentinela o procedimento é chamado de snoll.
As biópsias percutâneas podem ser a biópsia de agulha fina (um procedimento aspirativo, que permite exame citopatológico), as biópsias que permitem análise tecidual, a biópsia de fragmentos (também chamada de core biopsy e trucut) e a biópsia vacuoassistida (também chamada de mamotomia).
As formas de guiar a biópsia são a palpação (praticamente abandonada), a ultrassonografia, a mamografia e a ressonância magnética. Quando a lesão é vista à ultrassonografia, a preferência recai sobre ela. Quando ela é vista à mamografia a orientação pode ser de duas maneiras: estereotáxica (que usa um recurso adicionado a o mamógrafo, e que permite localização pré-operatória e biópsias percutâneas) ou biplanar (que permite apenas biópsias cirúrgicas, mas não requer o recurso da estereotaxia, que é consideravelmente caro). A biópsia orientada por ressonância magnética é reservada para as lesões que só foram demostradas por esse método, mesmo após cuidadosa revisão à ultrassonografia e à mamografia. Esse é um tipo de biópsia caro e pouco disponível em nosso meio.
A complexidade. O leitor deve ter percebido que as formas de combinação entre tipo de biópsia e forma de dirigir a biópsia leva a um grande número de opções (23 tipos de biópsia, para ser exato), e isso leva a uma grande complexidade para escolher a forma ideal de biópsia. Complexidade de escolha, de codificação, de autorização nos convênios, de comunicação com o radiologista, etc... Do outro lado está a paciente, numa das piores fases da sua vida, angustiada, afobada, querendo resolver. Daí a responsabilidade do solicitante em conhecer bem esse tema, para minimizar a possibilidade de glosas, não autorizações e outras situações que podem elevar o sofrimento da paciente.
A biópsia para cada tipo de lesão. Segue abaixo a escolha ideal para cada caso:
Nódulo: é a lesão mais comum. Melhor opção: biópsia de fragmentos orientada por ultrassonografia. Independente do tamanho do nódulo. A noção de que nódulos de tamanho pequeno seriam melhor biopsiados por biópsia vacuoassistida não se sustentou (a biópsia vacuoassistida é mais invasiva e não mostrou ser melhor; aliás, pode até ser pior, por provocar mais distorção tecidual, potencialmente aumentando o risco de não identificação da lesão durante o procedimento). Ocasionalmente nos deparamos com um nódulo cujas características à ultrassonografia não permitem diferenciar entre um nódulo sólido e um cisto com conteúdo espesso. Sendo esse o caso, é uma boa opção iniciar a abordagem com uma biópsia de agulha fina, pois caso o nódulo mostre ser cístico, a situação será resolvida com um mínimo de invasividade.
Microcalcificações: Segundo tipo de lesão mais comum. Melhor opção: biópsia vacuoassistida orientada por estereotaxia. Tem a desvantagem de ser menos disponível. Alternativa: biópsia de fragmentos orientada por estereotaxia, que tem a desvantagem de ter uma chance um pouco maior de erro de alvo e de subestimativa, mas é aceitável. Outra alternativa: biópsia cirúrgica sob localização pré-operatória (normalmente conhecida por agulhamento, que pode ser feito pela técnica biplanar e não exige estereotaxia). Em casos mais raros; as microcalcificações podem ter uma lesão correspondente visível à ultrassonografia. Nesses casos, preferir biópsia de fragmentos orientada por ultrassonografia, muito vantajosa pela menor invasividade e menor custo.
Distorções de arquitetura: Em geral preferir exérese cirúrgica. Algumas lesões pequenas podem ser abordadas com biópsia vacuoassistida ou, se tiverem uma correlação ultrassonográfica razoavelmente segura, pode ser tentado uma biópsia de fragmentos orientada por ultrassonografia. Quando não são vistas à ultrassonografia, que é a maior parte das vezes, a orientação tem que ser mamográfica, estereotáxica quando for realizada uma abordagem percutânea e biplanar quando for realizada uma abordagem cirúrgica.
Assimetrias: Se forem demonstradas à ultrassonografia, a opção ideal é a biópsia de fragmentos orientada por ultrassonografia. Na maioria das vezes, porém, as assimetrias só são vistas à mamografia e assim exigirão biópsia orientada por mamografia, seja orientação biplanar para realizar cirurgia sob agulhamento ou orientação estereotáxica para biópsia percutânea, simples ou vacuoassistida.
Lesões vistas apenas à ressonância magnética: Sempre que se encontra uma lesão suspeita à ressonância magnética, a primeira providência é voltar à ultrassonografia e até mesmo à mamografia para tentar procurar essa lesão de uma forma dirigida. Caso a lesão permaneça exclusiva da ressonância magnética, a biópsia terá que ser feita sob orientação desse método. Também nesse caso pode ser realizado um agulhamento com biópsia cirúrgica ou uma biópsia percutânea. Nesse caso, por causa do fato de que a orientação por ressonância magnética é um pouco menos precisa, é necessário usar a biópsia vacuoassistida, para remover mais material e garantir a amostragem. Além de pouco disponíveis, os procedimentos orientados por ressonância magnética requerem material (agulhas e fios) especial não ferromagnético, geralmente feitos de titânio.
Suspeita de carcinoma inflamatório: Na maioria das vezes é possível fazer uma biópsia de fragmentos orientada por ultrassonografia. No passado se falava de biópsias em cunha incluindo uma porção de derme para comprovar invasão linfática, mas hoje isso e desnecessário. O importante é confirmar a presença de carcinoma e o componente inflamatório é uma característica clínica.
Linfonodopatia axilar: Em geral a preferência é pela biópsia de agulha fina orientada por ultrassonografia, principalmente em função da dificuldade técnica relacionada à forma côncava da axila e às estruturas vasculares e neurais da axila. A biópsia de agulha fina é a que oferece maior controle ao operador, e para confirmação de envolvimento neoplásico em portadoras de câncer de mama tem acurácia excelente. Caso se suspeite de envolvimento linfonodal por neoplasias como linfomas ou melanomas, a melhor opção é a biópsia de fragmentos orientada por ultrassonografia.
Doença de Paget: Caso não haja lesão à ultrassonografia ou mamografia, a melhor opção é realizar uma biópsia em cunha da porção afetada da aréola.
Comentários finais. Dado a complexidade relatada acima, considere sempre discutir o caso com o imaginologista para otimizar a escolha do método de biópsia. Procura sempre ser claro no pedido, sobre qual lesão deve ser biopsiada e qual o tipo de biópsia escolhido. Procure preencher o pedido com clareza para evitar confusão na autorização da operadora (a complexidade também sobrecarrega a parte burocrática da biópsia e devemos evitar sofrimento adicional nesse momento já vulnerável para a paciente).
Autor: Hélio Sebastião Amâncio de Camargo Júnior
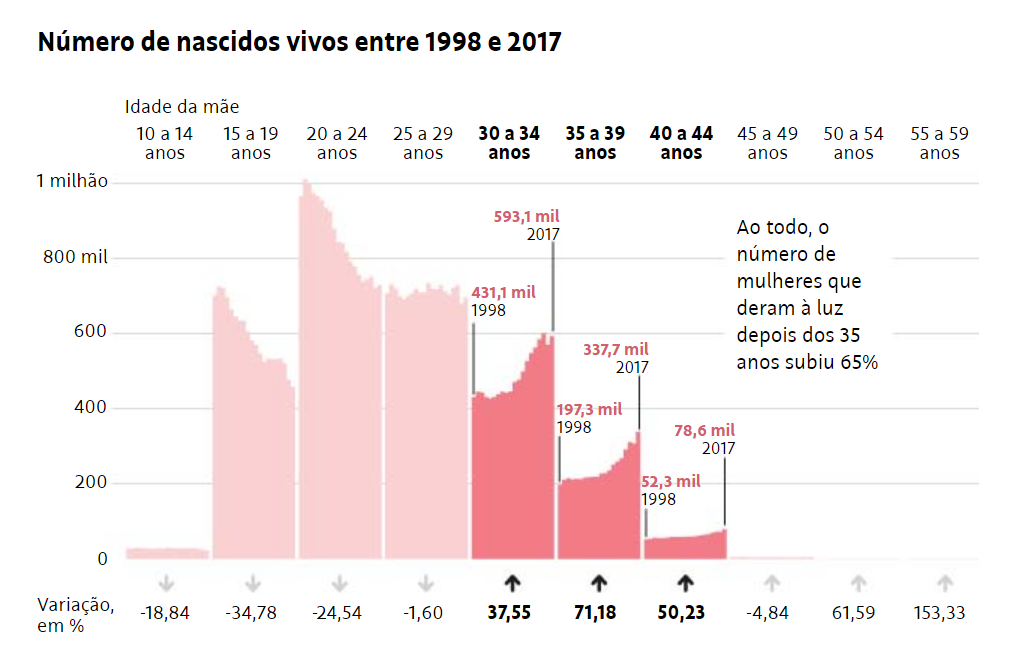
Em 20 anos, gravidez após os 35 anos cresce 65% no Brasil
Levantamento do núcleo de inteligência da Folha a partir dos dados do sistema de informações sobre nascidos vivos do Ministério da Saúde, aponta que o número de mulheres que deram à luz entre os 35 e os 39 anos aumentou 71% nos últimos anos no país.
De 1998 a 2017, o número de mulheres que deram à luz entre 40 e os 44 anos cresceu 50%. Dentre as que tiveram filhos dos 30 aos 34 anos, o aumento foi de 37%. Somadas as faixas acima dos 35 anos a alta 65%.
Leia o texto na íntegra com a participação do Dr. César Eduardo Fernandes (Presidente da FEBRASGO) clicado aqui.
Reprodução: Folha
Hormônios bioidênticos na pós-menopausa
A ideia de denominar substâncias hormonais semelhantes aos produzidos pelo próprio organismo como bioidênticas não é nova. Sua popularização ocorreu após as grandes personagens da mídia norte-americana divulgarem seu uso, inclusive inferindo qualidades que não foram comprovadas nos estudos clínicos (Taylor, 2001). Por isso, muitos investigadores ainda colocam em dúvida a superioridade da sua segurança e do seu efeito em relação a outros hormônios usualmente utilizados na terapia de reposição clássica, ou seja, os não bioidênticos (Holtorf, 2009; NAMS, 2012).
O termo bioidêntico na sua forma mais restrita é reservado, em geral, às substâncias de origem vegetal que tiveram modificação química em sua estrutura, tornando-se indistinguível dos hormônios humanos: a) estrogênio (17beta-estradiol, estrona e estriol); b) progesterona; c) androgênios (testosterona e deidroepiandrosterona) (Cirigliano, 2007). Salienta-se que estes compostos não incluem os fitohormônios. O bioidêntico contrasta com os estrogênios oriundos da urina de égua prenha e dos derivados sintéticos do estrogênio (promestrieno) e da progesterona (progestagênios). De forma mais ampla, Cirigliano (2007) considera ainda que os compostos que se tornam semelhantes ao hormônio original, também deve ser considerados como bioidênticos, como valerato e cipionato de estradiol e ésteres da testosterona.
Recentemente, alguns investigadores alegam que a melhor forma de ministrar o hormônio bioidêntico seria a via transdérmica. Além disso, sugerem monitoramento frequentemente, pela urina ou saliva, para avaliar os níveis hormonais. Esta prática é muito onerosa e os resultados podem ser questionáveis, pois ainda não sabemos o nível hormonal ideal para cada mulher (Fishman et al, 2015).
A percepção do termo bioidêntico para a população não é clara. Dois grandes inquéritos (Harris Interactive Inc e Rose Research LLC) foram utilizados para elaborar o relatório Symphony Health's Pharmaceutical Audit Suite (PHAST), que mostra as extrapolações e tendências de uso de diversos hormônios, incluindo os bioidênticos, na população americana. A maioria da população tem conceito equivocado e não detém informações confiáveis ou certeza se os hormônios bioidênticos têm aprovação do FDA. Além disso, uma parcela (27%) das participantes do estudo Rose, simplesmente não sabia nada sobre estes hormônios e o seu significado, bem como não tinham percepção se o resultado seria melhor do que com os demais tratamentos disponíveis.
O grande desafio com os hormônios bioidênticos é a individualização da dose a ser ministrada à paciente, pois há a necessidade de suporte laboratorial mais frequente e personalizado, o que aumentaria os custos enormemente sem necessariamente alcançar os objetivos do tratamento, ou seja, melhora dos sintomas. Não há comprovação científica que mostre que o seu uso, além de mais caro, traria mais benefícios às mulheres. Em geral, a dose padrão dos hormônios da terapia hormonal habitualmente prescrita pode ser mantida ou modificada conforme as queixas da mulher (Davison, 2009).
Assim, é importante assinalar que faltam evidências sobre sua real efetividade e segurança em mulheres na pós-menopausa em comparação com as terapêuticas hormonais não bioidênticas habitualmente empregadas.
Autor: Dr. Edmund Chada Baracat - Comissão Nacional Especializada em Ginecologia Endócrina
Referências Bibliográficas
- Fishman JR, Flatt MA, SetterstenRA.Bioidentical Hormones, Menopausal Women, and the Lure of the“Natural” in U.S. Anti-Aging Medicine.SocSci Med. 2015; 132: 79–87.
- Cirigliano M. Bioidentical hormone therapy: a review of the evidence. Journal of women’s health.2007; 16:600–631.
- Taylor M. Unconventional estrogens: estriol, biest, and triest. ClinObstet Gynecol. 2001;44(4):864-79.
- Holtorf K. The bioidentical hormone debate: are bioidentical hormones (estradiol, estriol, and progesterone) safer or more efficacious than commonly used synthetic versions in hormone replacement therapy? Postgrad Med. 2009;121(1):73-85.
- North American Menopause Society. The 2012 hormone therapy position statement
of: The North American Menopause Society. Menopause. 2012;19(3):257-71.
-
http://www.roseresearchcenter.com. Acesso em 10 de Outubro de 2016
-
http://symphonyhealth.com/product/pharmaceutical-audit-suite-phast. Acessoem 10 deOutobro de 2016
-
Davison S. Salivary testing opens a Pandora's box of issues surrounding accurate measurement of testosterone in women. Menopause. 2009;16(4):630-1.
Mamografia faz mal?
Surgem questionamentos sobre a prática médica em diferentes áreas da sociedade. Questiona-se o parto assistido por médicos, a forma tradicional de tratarmos as diferenças de gêneros, a ultrassonografia feita exclusivamente por médicos, o próprio conceito de ato médico e, naturalmente, a mamografia.
É claro que há exagero, despreparo e interesses escusos nessas críticas. Mas a melhor maneira de enfrentá-las é nos aprofundarmos nesses temas, ainda que sob o preço de sairmos da nossa zona de conforto. Questionar é bom. Nos faz refletir sobre as coisas que passamos a fazer automaticamente em nossas vidas. Mamografia é uma delas.
Sabemos o que a mamografia faz de bom. Ela salva vidas, reduzindo a mortalidade de mulheres assintomáticas que são efetivamente rastreadas em até 40% (Coldman, JNCI 2014;106).
Mas como tudo na vida há um outro lado dessa moeda. Ela também tem efeitos colaterais indesejados, que precisam ser conhecidos pelo médico solicitante. Quais são esses efeitos, e qual a sua magnitude?
A resposta a essa pergunta é o objetivo dessa comunicação. Abaixo estão listados todos os inconvenientes da mamografia. É importante conhecê-los para podermos orientar nossas pacientes adequadamente e escolhermos as melhores condutas médicas.
- A mamografia não é igualmente efetiva para todas as mulheres. Ela é menos eficaz em portadoras de mamas densas. Densidade é uma propriedade de cada mama, que significa falta de transparência à mamografia. Uma mamografia menos transparente esconde cânceres. Justamente numa população em que o risco de câncer de mama é maior. Uma pesquisa sueca mostrou um risco relativo de morte por câncer de mama de 1,91 em mulheres com mamas densas (Chiu, Cancer Epidemiol Biomarkers Prev 2010;19:1219), em parte pelo maior risco de câncer e em parte por atraso no diagnóstico.
- Embora a mamografia seja solicitada na mesma periodicidade que a colpocitologia oncótica por um longo período da vida da mulher, tendo esses dois exames a finalidade de rastrear os dois cânceres mais comuns das mulheres, a eficácia da mamografia para reduzir a mortalidade específica é muito menor que a do Papanicolaou. Enquanto a morte por câncer do colo uterino pode ser quase erradicada pelo rastreamento, não chegamos a prevenir nem a metade das mortes por câncer de mama.
- Nem tudo o que a mamografia vê é câncer. Significa dizer que há falsos positivos e biópsias desnecessárias. Quantas? Num bom serviço terá 2 a 3 biópsias positivas a cada 10 biópsias indicadas. Ou seja, 7 a 8 a cada 10 biópsias serão negativas, gerando o que chamamos de exame falso positivo. Em que pese o encontro de uma histologia benigna ser uma situação de desfecho alegre, todo o estresse da biópsia poderia nem sequer ter acontecido se a paciente não tivesse feito a mamografia. Vale lembrar que serviços de menor padrão de qualidade podem ter taxas de biópsias negativas bem maiores.
- Há uma limitação biológica. Um câncer pode crescer rápido demais, não ser visto em uma mamografia de rotina e tornar-se palpável e muitas vezes incurável antes da próxima mamografia de rotina. Chamamos a isso câncer de intervalo, que é uma das características do câncer agressivo. Mais uma vez encontramos uma limitação da mamografia em uma população que precisa mais dela, a das portadoras de tumores mais agressivos.
- Nem todo câncer diagnosticado significa uma vida salva. Essa observação mexe com nosso ego, que gosta de sentir que faz coisas importantes, mas é uma verdade essencial: descobrimos cânceres que nunca fariam mal àquela paciente. Permaneceriam indolentes ou até mesmo regridiriam. Pacientes são operadas, irradiadas e recebem quimioterapia desnecessariamente todos os dias. Essas situações são chamadas de sobrediagnóstico e sobre tratamento. Qual é a sua frequência? Esse número é de cálculo difícil, pois precisa precisa ser estimado com base em premissas incertas. Então ele é muito manipulável, servindo de crítica fácil para os detratores da mamografia, que chegam a estimá-lo em 50%, ou de argumento barato para os defensores incondicionais da mamografia, que chegam a dizer que sobrediagnóstico não existe. Pesquisas dentro de linhas bem equilibradas, porém, estimaram a taxa de sobre diagnóstico da mamografia em pouco menos de 10%.
- Os custos do rastreamento mamográfico não são negligenciáveis, especialmente se acrescidos dos custos das biópsias geradas e do controle de qualidade que é essencial para obter os resultados que justificam a realização do rastreamento. Parece fútil falar de custo de mamografia em um país que gasta tanto em estádios de futebol e parques olímpicos, mas queiramos ou não a racionalização dos custos é uma responsabilidade cidadã, de todos nós, e se a vida não pode ter um custo as intervenções de saúde têm.
- Existem muitas formas de biópsias. O desconhecimento pode levar à utilização de biópsias excessivamente agressivas para o caso em questão. É nossa responsabilidade ética usar sempre a forma menos agressiva de biópsia que forneça a informação desejada.
- Não! A mamografia não causa câncer de tireoide de forma significante. Vamos esquecer essa lenda urbana que foi criada e que não se sustenta factualmente.
Não sou contra a mamografia. Sou dos que acham que os inconvenientes relatados acima são um preço que vale a pena pagar pelas vidas salvas (embora salvas em número menos do que gostaríamos). Estou entre os que percebem que essas vidas, além de salvas, têm tratamento menos mutilante, pois feito em fase mais precoce. Esse tratamento menos mutilante não é um “endpoint” primário da mamografia e não é citado
Estou entre os que defendem o rastreamento mamográfico, mas assumindo a responsabilidade de informar à paciente todos os seus inconvenientes e limitações, de racionalizar o seu custo e invasividade, de manter uma expectativa realista. Minha experiência é que isso não demove as pacientes da vontade de participar de um programa de rastreamento.
Autor: Dr. Hélio Sebastião Amâncio de Camargo Júnior