Cuidados com a dosagem da gonadotrofina coriônica humana no seguimento de pacientes com Doença Trofoblástica Gestacional
Sexta, 16 Março 2018 15:01
A principal vigilância hormonal no seguimento pós-molar consiste na dosagem periódica e sistemática da gonadotrofina coriônica humana (hCG). Sendo um produto das células da placenta, em especial do sinciciotrofoblasto, o hCG também é secretado em menores quantidades pelas células citotrofoblásticas. O hCG pertence ao grupo dos hormônios glicoproteicos, que também compreende o luteinizante (LH), o folículo-estimulante (FSH) e o tireoestimulante (TSH). Todos estes possuem duas subunidades diferentes, a e b, que são unidas por ligações não covalentes e que precisam estar combinadas para formar o hormônio biologicamente ativo. A subunidade a é produzida tanto na hipófise como na placenta e tem a mesma seqüência peptídica das subunidades a de outros hormônios (LH, FSH, TSH). A subunidade b é peculiar a cada hormônio e determina sua especificidade.
O hCG é produzido pela placenta na gestação normal, pela doença trofoblástica gestacional (DTG), em mulheres que estão ou estiveram grávidas, nas neoplasias de origem germinativa, por tumores não-trofoblásticos e também em tecidos normais, incluindo testículo e hipófise humana. A principal função do hCG é promover a produção de progesterona pelo corpo lúteo do ovário.
No início da gestação normal, o trofoblasto se diferencia em células predominantemente citotrofoblásticas, enquanto as células sinciciotrofoblásticas são dominantes ao término da gravidez. O sinciciotrofoblasto é a maior fonte secretora de hCG intacto na circulação materna e as células menos diferenciadas do citotrofoblasto secretam além do hormônio na sua forma intacta, as subunidades a e b. À semelhança da placenta normal, as células anormais do trofoblasto na doença trofoblástica gestacional (DTG) sintetizam e secretam tanto o hCG intacto como as formas livres das subunidades a e b.
Após 1980, foram desenvolvidos imunoensaios tipo sanduíche, rápidos e automatizados, usando anticorpos monoclonais para reconhecer especificamente o hCG e suas subunidades livres. Tais ensaios, que são tão ou mais sensíveis do que o teste do b-hCG por radioimunoensaio, não utilizam radioisótopos, apresentam menor coeficiente de variação e maior durabilidade dos reagentes, o que implica um menor custo final na execução do exame. As diferentes formas degradadas do hCG são reconhecidas por um grande número de anticorpos, o que resulta em grande variação nos resultados inter-ensaios, especialmente se a determinação é na urina, trazendo confusão nos resultados dos testes para diagnóstico de gravidez. Utilizam-se amostras séricas para fins de monitorização dos níveis de hCG durante a gravidez (tratamento conservador e medicamentoso da gravidez ectópica e na fertilização assistida) e na monitorização das neoplasias, em especial a Neoplasia Trofoblástica Gestacional (NTG).
A natureza complexa dos produtos de degradação do hCG intacto, da meia-vida dos produtos de degradação e das reações cruzadas dos vários produtos de degradação com os vários anticorpos, explica a discrepância entre os resultados da dosagem de gonadotrofina coriônica feita nos diferentes laboratórios e, num mesmo laboratório, com o mesmo kit, entre as diferentes amostras do material.
Atualmente, a conduta efetiva dos casos de DTG é altamente dependente da determinação do imunoensaio sérico para dosagem quantitativa do hCG, que deve ser utilizado em todos os estágios do manejo da DTG, incluindo diagnóstico, planejamento terapêutico, monitorização da resposta ao tratamento e detecção das eventuais recidivas. Em DTG é recomendável um ensaio que dose o hCG total + b hCG, que tem a vantagem de reconhecer também o hCG clivado e o b- hCG-clivado, o que proporcionará resultados mais precisos e condutas clínicas mais acertadas.
O uso do hCG apenas na propedêutica da DTG é direcionado para cinco momentos: 1) Diagnóstico de DTG; 2) Seguimento pós-esvaziamento molar; 3) Diagnóstico de Neoplasia Trofoblástica Gestacional pós-molar 4) Monitorização do tratamento quimioterápico; 5) Diagnóstico de recidiva da NTG.
Para os fins acima referidos é indispensável a determinação quantitativa de b-hCG (hCG intacto + b-hCG), exames que preferencialmente devem ser realizados em um mesmo laboratório, para se ter credibilidade e se poder comparar o resultado com outros da mesma procedência. É importante também que os profissionais do laboratório onde o exame é realizado tenham conhecimento que lidam com um marcador tumoral e que os resultados se destinam à monitorização de DTG, e não apenas ao diagnóstico de gravidez, ou seja, ratificando a necessidade de o resultado ser precisamente quantificado.
hCG no diagnóstico de DTG
Em condições normais da gestação, os níveis séricos de hCG biologicamente ativo aumentam exponencialmente no 1º trimestre da gravidez, duplicando a cada dois dias, atingindo o pico em torno da 10ª -12a semanas, quando podem alcançar valores de 100.000 mUI/mL. A partir daí os valores decrescem até a 20ª semana, atingindo cerca de 20% dos valores de pico máximo e assim permanecem até o final da gestação. Após o parto os níveis séricos de hCG seguem regredindo e os resultados dos testes atingem valores normais (<5 mUI/mL) em torno de 30 dias.
Após a interrupção de uma gravidez não-molar na 1a metade da gestação, os valores de hCG atingem resultado normal em torno de 2 a 3 semanas. Essa informação é importante por auxiliar a conduta clínica frente à paciente que tenha apresentado um abortamento espontâneo e completo, e/ou quando um exame anátomo-patológico for inconclusivo no diagnóstico de Mola Hidatiforme (MH) (quando, por exemplo, evidenciar apenas edema de vilos sem hiperplasia de trofoblasto), situação em que uma dosagem de hCG feita em 3 semanas ajuda a elucidar o diagnóstico: se nesse tempo referido acima a dosagem sérica do hCG for < 5 mUI/mL fica afastado uma DTG e o edema de vilos deve refletir outras cromossomopatias.
Na mulher em idade fértil e sem uso de contraceptivos, frente a um resultado positivo de hCG, a maior probabilidade é se tratar de uma gravidez normal. Diante de um atraso menstrual, se uma paciente com hCG positivo apresentar sangramento genital e um exame de ultra-sonografia (US) mostrando conteúdo uterino sugestivo de MH, uma dosagem de hCG sérico quantitativo com valores elevados confirma a suspeita de DTG. Na MH parcial, situação na qual os valores séricos quantitativos do hCG são geralmente menos elevados, o diagnóstico clínico e US inicialmente é de gestação interrompida; para um diagnóstico precoce de MH parcial destaca-se a importância do exame histológico sistemático de todo material curetado, com alerta ao patologista se houver suspeita diagnóstica de MH parcial.
A realização de uma dosagem de hCG é também importante no diagnóstico diferencial de miomas uterinos intracavitários (submucosos) com degeneração: a imagem ao US dessa patologia, por vezes, é sugestiva de MH. Se a dosagem de hCG for negativa é afastada uma gravidez e fica reforçada a suspeita inicial de mioma degenerado.
A dosagem de hCG também é essencial no rastreamento de causas de sangramento uterino disfuncional ou em mulheres que, no menacme, mesmo sem sangramento anormal, apresentem sintomas atípicos como hemoptise, dores abdominais, convulsões, etc.; nestes casos, na ausência de gestação documentada há mais de 30 dias, um hCG positivo levanta a hipótese de DTG e indica avaliação diagnóstica.
Para diagnóstico de gestação molar basta um resultado positivo na dosagem de hCG (≥ 200 mUI/mL) associado à imagem típica ao US. A quantificação do hCG nessa etapa diagnóstica será relevante, entretanto, para identificação da MH de alto-risco para desenvolvimento de NTG; em tais pacientes uma dosagem de hCG ≥ 100.000 mUI/ml é sinal de alerta para rastreio das complicações médicas associadas ao hCG elevado, tais como tamanho uterino maior do que o esperado para a idade gestacional, presença de cistos ovarianos teca-luteínicos volumosos, pré-eclampsia, hipertiroidismo e embolização trofoblástica.
Na quantificação do hCG é importante também destacar a possibilidade de um resultado falsamente mais baixo devido ao efeito “hook”, que pode estar presente quando os níveis da gonadotrofina são extremamente elevados. O excesso de hCG progressivamente satura a fase sólida e a detecção de anticorpos, impedindo que haja formação do “sanduíche” que quantifica o hCG, quando se utilizam os novos ensaios com anticorpos monoclonais. Esse efeito pode ser prevenido pela diluição da amostra a 1/100 e 1/10000. Frente à paciente com gestação molar e úteros volumosos, um contato da equipe médica com o laboratório torna-se essencial, antes de ser iniciado o processo de quantificação do hCG, para evitar os resultados incorretos
O valor do b hCG obtido antes ou logo após esvaziamento da MH representa o ponto inicial de uma curva onde serão colocadas sucessivamente a cada 7 dias os outros valores numéricos, configurando a curva individual de regressão do b hCG, que possibilita identificar precocemente a evolução da DTG para remissão espontânea ou para evolução neoplásica.
hCG no acompanhamento pós- molar
Feito um diagnóstico clínico de MH, o próximo passo é o esvaziamento da cavidade uterina, preferencialmente com o método de vácuo-aspiração elétrica ou manual, através do qual se consegue o material para ser enviado para exame histopatológico. Segue tal procedimento cirúrgico, um acompanhamento com consultas médicas e dosagens quantitativas de hCG, que duram em média 6 a 8 meses, conhecido como acompanhamento pós-molar. Esse acompanhamento que deve ser realizado preferencialmente em Centros de Referência (CR), onde uma equipe multidisciplinar treinada proporcione o atendimento adequado em todas as fases do tratamento. Nessa etapa, o b-hCG, que precisa sempre ser precisamente quantificado, tem papel relevante como marcador tumoral.
Recomenda-se que as pacientes façam consultas médicas acompanhadas da dosagem de b-hCG até serem obtidos três resultados semanais consecutivos com níveis inferiores a 5 mUI/mL quando, por definição clínica, é caracterizada a remissão da doença. Após a remissão, o controle passa a ser mensal, durante mais cerca de 6 meses. Durante todo o seguimento pós-molar as pacientes devem fazer anticoncepção rigorosa, de preferência mediante o uso de anticoncepcional oral, uma vez que não podem engravidar durante o período de acompanhamento. A anticoncepção eficaz é um dos pilares do controle pós-molar e como tal, o uso é recomendado e garantido. A maioria das pacientes portadoras de MH (80%) permanece assintomática até a cura completa da doença.
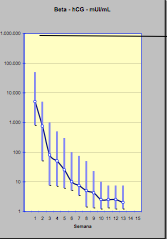
A curva de regressão do b-hCG de cada paciente realizada durante o acompanhamento pós-molar pode ser comparada com a curva semi-logarítmica e exponencial de regressão normal do hCG, conforme proposto por Schlaerth et al (Figura 2) ou com outra proposta em nosso meio por Maestá. Se os valores forem progressivamente descendentes e paralelos à curva padrão de regressão significa que a paciente está evoluindo para remissão espontânea da doença, dispensando qualquer tratamento adicional. (Figura 3).
O objetivo principal do acompanhamento pós-molar identificar precocemente as pacientes com evolução para NTG (prevenção secundária). Para tanto, a dosagem sérica quantitativa de hCG é recurso propedêutico imprescindível por traduzir a quantidade de trofoblasto remanescente.
Está sendo questionada a duração do seguimento pós- remissão, em especial nos casos de MH Parcial, quando então alguns autores sugerem que o seguimento encerre ao ser atingida a remissão da DTG.
hCG no diagnóstico de NTG pós-molar
As vezes a presença de sinais e sintomas clínicos (sangramento transvaginal), e mais comumente a persistência de níveis elevados de b-hCG associado ou não a evidência de infiltração na parede uterina pela US (área de lesão ou vascularização aumentada) são a base do diagnóstico de NTG, que compreende a mola invasora, o coriocarcinoma, o tumor placentário do sítio placentário e o tumor trofoblástico epitelióide.
A mola invasora, que é a forma mais freqüente de NTG, representa a evolução maligna da mola hidatiforme, e pode ter apenas diagnóstico químico traduzido pela persistência dos valores altos de b-hCG após o esvaziamento molar. Em torno de 20% das pacientes no controle pós-molar desenvolvem a NTG, que se refere aos tipos de DTG que necessitam de tratamento adicional com quimioterapia (Qt) para ser alcançada a remissão da neoplasia.
Na maior parte dos casos que complicam, o diagnóstico precoce pode ser feito através da análise da curva de regressão individual da gonadotrofina coriônica. Se os níveis do hCG ficarem ascendentes por 2 semanas consecutivas ou em plateau no mínimo por 3 semanas consecutivas, faz-se hipótese diagnóstica de evolução complicada para neoplasia, e estará indicada uma avaliação metastática, para definir o estadiamento clínico da Federação Internacional de Ginecologia e Obstetrícia (FIGO), bem como o escore de risco para resistência ao tratamento quimioterápico, proposto pela Organização Mundial da Saúde (OMS), a fim de se planejar o tratamento mais indicado a cada caso.
Devido à lentidão com que os níveis de b-hCG podem decrescer, está estabelecido em alguns protocolos a não utilização de Qt enquanto esses valores forem descendentes, mantendo-se a vigilância ativa. Se os níveis de hCG forem baixos e não houver lesão detectada no rastreamento da doença complicada, a conduta indicada pela FIGO é manter ainda o seguimento com dosagem de hCG a cada 15 dias, sem tratamento Qt, até serem atingidas as 24 semanas pós-esvaziamento uterino, quando então fica caracterizado outro critério da FIGO para indicar Qt.
Quanto à regressão dos níveis de b-hCG, é citado que 36% das mulheres com valores elevados no 60º dia pós-esvaziamento evoluem, posteriormente, para mola invasora ou coriocarcinoma. Torna-se, portanto, imprescindível que a paciente seja mantida em rigoroso acompanhamento até a definição diagnóstica, com vistas à terapêutica precoce e adequada.
Na vigência de sangramento anormal após abortamento não-molar, gravidez ectópica ou de gestação a termo, a gonadotrofina coriônica também deve ser pesquisada com vistas a um possível diagnóstico de coriocarcinoma.
Resultados falso-positivos de hCG têm induzido o tratamento de pacientes que em realidade não se apresentavam com a forma resistente da doença. Um falso-positivo se deve à presença de anticorpos heterofílicos nas amostras séricas, caracterizando o b-hCG “fantasma”, cuja presença pode ser afastada mediante a pesquisa de hCG na urina. Se o hCG for positivo tanto no sangue quanto na urina não se trata de “hCG fantasma”.
O acompanhamento de casos de DTG com valores de b-hCG baixos (<200 mUI/mL) e persistentes (período de 3 meses), sem lesões identificáveis pelos métodos de imagem, leva ao diagnóstico de DTG quiescente. Verificou-se que existem pacientes que evoluem nessas condições durante vários anos, mas 11% dessas pacientes subitamente apresentam níveis de b-hCG crescentes, com identificação de lesões complementares.
Pacientes com níveis de b-hCG baixos e persistentes configuram três situações distintas: a) havendo história anterior de DTG, a situação é classificada como DTG quiescente; b) sem antecedente de DTG, é configurada uma elevação inexplicada de hCG e c) os casos falso-positivos, também chamados de “hCG fantasma”.
hCG na monitorização do tratamento quimioterápico
Durante a monitorização do tratamento com Qt é essencial a manutenção das dosagens quantitativas e semanais de hCG. A resposta adequada à Qt é facilmente verificada pela análise da curva de regressão do hCG, a qual regride paralelamente à curva padrão. Entretanto, se estiver se desenvolvendo resistência ao agente quimioterápico utilizado, os valores do hCG voltam a ficar em plateau ou ascendentes, o que indica mudança de esquema de Qt.
Vale destacar que, no início do tratamento com qualquer fármaco quimioterápico, freqüentemente se observa um pequeno aumento nos valores séricos do hCG porque, devido à lise das células tumorais, ocorre mais liberação de gonadotrofina coriônica na circulação sanguínea, refletida pelo aumento inicial no hCG.
hCG no diagnóstico de NTG recidivante
A manutenção do controle do hCG precisa persistir após o final do tratamento com ou sem Qt, com a finalidade de precocemente ser diagnosticada uma recidiva de NTG
Após a remissão da NTG, momento em que se iniciam os ciclos de reforço ou consolidação do tratamento com Qt, as dosagens de hCG devem seguir sendo realizadas a cada 15 dias, até o final das séries de Qt e recuperação hematológica.
A recidiva da NTG varia de menos de 5% a 20%, de acordo com o estadiamento da FIGO, respectivamente nos estádios I e IV. Considerando que 80% das recidivas de NTG acontecem nos primeiros 3 meses após a remissão, nesse período a dosagem de hCG precisa ser feita a cada 15 dias. Após esses 3 meses, o controle laboratorial do hCG passa a ser mensal por mais 6 meses e depois a cada 60 dias, por mais 6 meses.
O grupo liderado por Bagshawe recomenda posteriormente um controle semestral de hCG, até completar 5 anos da remissão, momento em que as pacientes com NTG não-metastática recebem alta do acompanhamento. Também recomendam que as pacientes com NTG metastática ou com diagnóstico de coriocarcinoma permaneçam com dosagem anual da gonadotrofina coriônica por um tempo indefinido, pelo risco mínimo, porém existente, de reativação tardia. Informações recentes (Seckl M; XIX World Congresso on GTD, Amsterdam, 2017) sugerem que esse controle tardio pode ser encerrado 7 anos após a remissão.
Leitura suplementar
Harvey RA. Measurement of human Chorionic Gonadotrophin (hCG) in the management of trophoblastic disease. In: Hancock BW, Seckl MJ and Berkowitz RS eds. Gestational Trophoblastic Disease – 4th edition, 2015, chapter 5- www/isstd/org
Uberti EMH, Diestel MCF, Campestrini DT et al. Importância e dificuldades na quantificação do bHCG em pacientes com Doença Trofoblástica Gestacional. GO Atual 1999;8(9):8-18.
Vartiainen J, Alfthan H, Lehtovirta P et al. Elevated hCG and a high proportion of hCG b in serum preceding the diagnosis of trophoblastic disease by seven months. Br J Obstet Gynaecol RCOG 2002;109:589-90.
Levavi H, Neri A, Bar J et al. “Hook effect” in complete hydatidiform molar pregnancy: a falsely low level of b-hCG. Obstet Gynecol 1993; 82:720-1.
Schlaerth JB, Morrow CP, Kletzky AO, et al. Prognostic characteristics of serum human chorionic gonadotropin titer regression following Molar Pregnancy. Obstet Gynecol 1981;50:478-82.
Maestá I, Rudge MVC, Passos JRS et al. Características das curvas de regressão da gonadotrofina coriônica pós-Mola Hidatiforme completa. RBGO 2000; 22(6):373-80.
Feltmate CM, Batorfi J, Fulop V et al. Human chorionic gonadotropin follow-up in patients with molar pregnancy: a time for reevaluation. Obstet Gynecol 2003; 101:732-6.
Kohorn EI. Persistent low-level “real” human chorionic gonadotropin: a clinical challenge and a therapeutic dilemma. Gynecol Oncol 2002; 85:315-20.
ACOG Committee Opinion nº 278. Avoiding inappropriate clinical decisions based on false-positive human chorionic test results. Obstet Gynecol 2002;100:1057-9.
Bagshawe KD. Choriocarcinoma: a model for tumour markers. Acta Oncol 1992;31:99-106.
Surwit EA, Hammond CB. Recurrent Gestational Trophoblastic Disease. Gynecol Oncol 1981; 12:177-85.
Souza JMQ, Braga A, Santos RS, Ramos MM, Cortez-Charry R, Maesta I. Comparison of two human chorionic gonadotropin immunoassay commercially available for monitoring patients with gestational trophoblastic disease. Int J Gynecol Cancer. 2017 Sep;27(7):1494-1500.
Comissão Nacional Especializada em Doença Trofoblástica Gestacional
FEBRASGO
Gestão 2016-2018
Elza Uberti, José Mauro Madi, Antonio Braga, Bruno Grillo, Maurício Viggiano,
Izildinha Maestá, Jurandyr Moreira de Andrade, Sue Sun, Rita de Cássia Ferreira
O hCG é produzido pela placenta na gestação normal, pela doença trofoblástica gestacional (DTG), em mulheres que estão ou estiveram grávidas, nas neoplasias de origem germinativa, por tumores não-trofoblásticos e também em tecidos normais, incluindo testículo e hipófise humana. A principal função do hCG é promover a produção de progesterona pelo corpo lúteo do ovário.
No início da gestação normal, o trofoblasto se diferencia em células predominantemente citotrofoblásticas, enquanto as células sinciciotrofoblásticas são dominantes ao término da gravidez. O sinciciotrofoblasto é a maior fonte secretora de hCG intacto na circulação materna e as células menos diferenciadas do citotrofoblasto secretam além do hormônio na sua forma intacta, as subunidades a e b. À semelhança da placenta normal, as células anormais do trofoblasto na doença trofoblástica gestacional (DTG) sintetizam e secretam tanto o hCG intacto como as formas livres das subunidades a e b.
 |
|||
|
|||
Após 1980, foram desenvolvidos imunoensaios tipo sanduíche, rápidos e automatizados, usando anticorpos monoclonais para reconhecer especificamente o hCG e suas subunidades livres. Tais ensaios, que são tão ou mais sensíveis do que o teste do b-hCG por radioimunoensaio, não utilizam radioisótopos, apresentam menor coeficiente de variação e maior durabilidade dos reagentes, o que implica um menor custo final na execução do exame. As diferentes formas degradadas do hCG são reconhecidas por um grande número de anticorpos, o que resulta em grande variação nos resultados inter-ensaios, especialmente se a determinação é na urina, trazendo confusão nos resultados dos testes para diagnóstico de gravidez. Utilizam-se amostras séricas para fins de monitorização dos níveis de hCG durante a gravidez (tratamento conservador e medicamentoso da gravidez ectópica e na fertilização assistida) e na monitorização das neoplasias, em especial a Neoplasia Trofoblástica Gestacional (NTG).
A natureza complexa dos produtos de degradação do hCG intacto, da meia-vida dos produtos de degradação e das reações cruzadas dos vários produtos de degradação com os vários anticorpos, explica a discrepância entre os resultados da dosagem de gonadotrofina coriônica feita nos diferentes laboratórios e, num mesmo laboratório, com o mesmo kit, entre as diferentes amostras do material.
Atualmente, a conduta efetiva dos casos de DTG é altamente dependente da determinação do imunoensaio sérico para dosagem quantitativa do hCG, que deve ser utilizado em todos os estágios do manejo da DTG, incluindo diagnóstico, planejamento terapêutico, monitorização da resposta ao tratamento e detecção das eventuais recidivas. Em DTG é recomendável um ensaio que dose o hCG total + b hCG, que tem a vantagem de reconhecer também o hCG clivado e o b- hCG-clivado, o que proporcionará resultados mais precisos e condutas clínicas mais acertadas.
O uso do hCG apenas na propedêutica da DTG é direcionado para cinco momentos: 1) Diagnóstico de DTG; 2) Seguimento pós-esvaziamento molar; 3) Diagnóstico de Neoplasia Trofoblástica Gestacional pós-molar 4) Monitorização do tratamento quimioterápico; 5) Diagnóstico de recidiva da NTG.
Para os fins acima referidos é indispensável a determinação quantitativa de b-hCG (hCG intacto + b-hCG), exames que preferencialmente devem ser realizados em um mesmo laboratório, para se ter credibilidade e se poder comparar o resultado com outros da mesma procedência. É importante também que os profissionais do laboratório onde o exame é realizado tenham conhecimento que lidam com um marcador tumoral e que os resultados se destinam à monitorização de DTG, e não apenas ao diagnóstico de gravidez, ou seja, ratificando a necessidade de o resultado ser precisamente quantificado.
hCG no diagnóstico de DTG
Em condições normais da gestação, os níveis séricos de hCG biologicamente ativo aumentam exponencialmente no 1º trimestre da gravidez, duplicando a cada dois dias, atingindo o pico em torno da 10ª -12a semanas, quando podem alcançar valores de 100.000 mUI/mL. A partir daí os valores decrescem até a 20ª semana, atingindo cerca de 20% dos valores de pico máximo e assim permanecem até o final da gestação. Após o parto os níveis séricos de hCG seguem regredindo e os resultados dos testes atingem valores normais (<5 mUI/mL) em torno de 30 dias.
Após a interrupção de uma gravidez não-molar na 1a metade da gestação, os valores de hCG atingem resultado normal em torno de 2 a 3 semanas. Essa informação é importante por auxiliar a conduta clínica frente à paciente que tenha apresentado um abortamento espontâneo e completo, e/ou quando um exame anátomo-patológico for inconclusivo no diagnóstico de Mola Hidatiforme (MH) (quando, por exemplo, evidenciar apenas edema de vilos sem hiperplasia de trofoblasto), situação em que uma dosagem de hCG feita em 3 semanas ajuda a elucidar o diagnóstico: se nesse tempo referido acima a dosagem sérica do hCG for < 5 mUI/mL fica afastado uma DTG e o edema de vilos deve refletir outras cromossomopatias.
Na mulher em idade fértil e sem uso de contraceptivos, frente a um resultado positivo de hCG, a maior probabilidade é se tratar de uma gravidez normal. Diante de um atraso menstrual, se uma paciente com hCG positivo apresentar sangramento genital e um exame de ultra-sonografia (US) mostrando conteúdo uterino sugestivo de MH, uma dosagem de hCG sérico quantitativo com valores elevados confirma a suspeita de DTG. Na MH parcial, situação na qual os valores séricos quantitativos do hCG são geralmente menos elevados, o diagnóstico clínico e US inicialmente é de gestação interrompida; para um diagnóstico precoce de MH parcial destaca-se a importância do exame histológico sistemático de todo material curetado, com alerta ao patologista se houver suspeita diagnóstica de MH parcial.
A realização de uma dosagem de hCG é também importante no diagnóstico diferencial de miomas uterinos intracavitários (submucosos) com degeneração: a imagem ao US dessa patologia, por vezes, é sugestiva de MH. Se a dosagem de hCG for negativa é afastada uma gravidez e fica reforçada a suspeita inicial de mioma degenerado.
A dosagem de hCG também é essencial no rastreamento de causas de sangramento uterino disfuncional ou em mulheres que, no menacme, mesmo sem sangramento anormal, apresentem sintomas atípicos como hemoptise, dores abdominais, convulsões, etc.; nestes casos, na ausência de gestação documentada há mais de 30 dias, um hCG positivo levanta a hipótese de DTG e indica avaliação diagnóstica.
Para diagnóstico de gestação molar basta um resultado positivo na dosagem de hCG (≥ 200 mUI/mL) associado à imagem típica ao US. A quantificação do hCG nessa etapa diagnóstica será relevante, entretanto, para identificação da MH de alto-risco para desenvolvimento de NTG; em tais pacientes uma dosagem de hCG ≥ 100.000 mUI/ml é sinal de alerta para rastreio das complicações médicas associadas ao hCG elevado, tais como tamanho uterino maior do que o esperado para a idade gestacional, presença de cistos ovarianos teca-luteínicos volumosos, pré-eclampsia, hipertiroidismo e embolização trofoblástica.
Na quantificação do hCG é importante também destacar a possibilidade de um resultado falsamente mais baixo devido ao efeito “hook”, que pode estar presente quando os níveis da gonadotrofina são extremamente elevados. O excesso de hCG progressivamente satura a fase sólida e a detecção de anticorpos, impedindo que haja formação do “sanduíche” que quantifica o hCG, quando se utilizam os novos ensaios com anticorpos monoclonais. Esse efeito pode ser prevenido pela diluição da amostra a 1/100 e 1/10000. Frente à paciente com gestação molar e úteros volumosos, um contato da equipe médica com o laboratório torna-se essencial, antes de ser iniciado o processo de quantificação do hCG, para evitar os resultados incorretos
O valor do b hCG obtido antes ou logo após esvaziamento da MH representa o ponto inicial de uma curva onde serão colocadas sucessivamente a cada 7 dias os outros valores numéricos, configurando a curva individual de regressão do b hCG, que possibilita identificar precocemente a evolução da DTG para remissão espontânea ou para evolução neoplásica.
hCG no acompanhamento pós- molar
Feito um diagnóstico clínico de MH, o próximo passo é o esvaziamento da cavidade uterina, preferencialmente com o método de vácuo-aspiração elétrica ou manual, através do qual se consegue o material para ser enviado para exame histopatológico. Segue tal procedimento cirúrgico, um acompanhamento com consultas médicas e dosagens quantitativas de hCG, que duram em média 6 a 8 meses, conhecido como acompanhamento pós-molar. Esse acompanhamento que deve ser realizado preferencialmente em Centros de Referência (CR), onde uma equipe multidisciplinar treinada proporcione o atendimento adequado em todas as fases do tratamento. Nessa etapa, o b-hCG, que precisa sempre ser precisamente quantificado, tem papel relevante como marcador tumoral.
Recomenda-se que as pacientes façam consultas médicas acompanhadas da dosagem de b-hCG até serem obtidos três resultados semanais consecutivos com níveis inferiores a 5 mUI/mL quando, por definição clínica, é caracterizada a remissão da doença. Após a remissão, o controle passa a ser mensal, durante mais cerca de 6 meses. Durante todo o seguimento pós-molar as pacientes devem fazer anticoncepção rigorosa, de preferência mediante o uso de anticoncepcional oral, uma vez que não podem engravidar durante o período de acompanhamento. A anticoncepção eficaz é um dos pilares do controle pós-molar e como tal, o uso é recomendado e garantido. A maioria das pacientes portadoras de MH (80%) permanece assintomática até a cura completa da doença.
A curva de regressão do b-hCG de cada paciente realizada durante o acompanhamento pós-molar pode ser comparada com a curva semi-logarítmica e exponencial de regressão normal do hCG, conforme proposto por Schlaerth et al (Figura 2) ou com outra proposta em nosso meio por Maestá. Se os valores forem progressivamente descendentes e paralelos à curva padrão de regressão significa que a paciente está evoluindo para remissão espontânea da doença, dispensando qualquer tratamento adicional. (Figura 3).
 |
||||
|
||||
| Figura 3: Curva de regressão do hCG de uma paciente com gestação molar e evolução para remisão espontânea, com regressão dentro dos limites do desvio padrão da curva padrão de regressão proposta por Schlaerth et al40 | 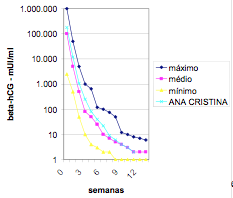 |
|||
O objetivo principal do acompanhamento pós-molar identificar precocemente as pacientes com evolução para NTG (prevenção secundária). Para tanto, a dosagem sérica quantitativa de hCG é recurso propedêutico imprescindível por traduzir a quantidade de trofoblasto remanescente.
Está sendo questionada a duração do seguimento pós- remissão, em especial nos casos de MH Parcial, quando então alguns autores sugerem que o seguimento encerre ao ser atingida a remissão da DTG.
hCG no diagnóstico de NTG pós-molar
As vezes a presença de sinais e sintomas clínicos (sangramento transvaginal), e mais comumente a persistência de níveis elevados de b-hCG associado ou não a evidência de infiltração na parede uterina pela US (área de lesão ou vascularização aumentada) são a base do diagnóstico de NTG, que compreende a mola invasora, o coriocarcinoma, o tumor placentário do sítio placentário e o tumor trofoblástico epitelióide.
A mola invasora, que é a forma mais freqüente de NTG, representa a evolução maligna da mola hidatiforme, e pode ter apenas diagnóstico químico traduzido pela persistência dos valores altos de b-hCG após o esvaziamento molar. Em torno de 20% das pacientes no controle pós-molar desenvolvem a NTG, que se refere aos tipos de DTG que necessitam de tratamento adicional com quimioterapia (Qt) para ser alcançada a remissão da neoplasia.
Na maior parte dos casos que complicam, o diagnóstico precoce pode ser feito através da análise da curva de regressão individual da gonadotrofina coriônica. Se os níveis do hCG ficarem ascendentes por 2 semanas consecutivas ou em plateau no mínimo por 3 semanas consecutivas, faz-se hipótese diagnóstica de evolução complicada para neoplasia, e estará indicada uma avaliação metastática, para definir o estadiamento clínico da Federação Internacional de Ginecologia e Obstetrícia (FIGO), bem como o escore de risco para resistência ao tratamento quimioterápico, proposto pela Organização Mundial da Saúde (OMS), a fim de se planejar o tratamento mais indicado a cada caso.
Devido à lentidão com que os níveis de b-hCG podem decrescer, está estabelecido em alguns protocolos a não utilização de Qt enquanto esses valores forem descendentes, mantendo-se a vigilância ativa. Se os níveis de hCG forem baixos e não houver lesão detectada no rastreamento da doença complicada, a conduta indicada pela FIGO é manter ainda o seguimento com dosagem de hCG a cada 15 dias, sem tratamento Qt, até serem atingidas as 24 semanas pós-esvaziamento uterino, quando então fica caracterizado outro critério da FIGO para indicar Qt.
Quanto à regressão dos níveis de b-hCG, é citado que 36% das mulheres com valores elevados no 60º dia pós-esvaziamento evoluem, posteriormente, para mola invasora ou coriocarcinoma. Torna-se, portanto, imprescindível que a paciente seja mantida em rigoroso acompanhamento até a definição diagnóstica, com vistas à terapêutica precoce e adequada.
Na vigência de sangramento anormal após abortamento não-molar, gravidez ectópica ou de gestação a termo, a gonadotrofina coriônica também deve ser pesquisada com vistas a um possível diagnóstico de coriocarcinoma.
Resultados falso-positivos de hCG têm induzido o tratamento de pacientes que em realidade não se apresentavam com a forma resistente da doença. Um falso-positivo se deve à presença de anticorpos heterofílicos nas amostras séricas, caracterizando o b-hCG “fantasma”, cuja presença pode ser afastada mediante a pesquisa de hCG na urina. Se o hCG for positivo tanto no sangue quanto na urina não se trata de “hCG fantasma”.
O acompanhamento de casos de DTG com valores de b-hCG baixos (<200 mUI/mL) e persistentes (período de 3 meses), sem lesões identificáveis pelos métodos de imagem, leva ao diagnóstico de DTG quiescente. Verificou-se que existem pacientes que evoluem nessas condições durante vários anos, mas 11% dessas pacientes subitamente apresentam níveis de b-hCG crescentes, com identificação de lesões complementares.
Pacientes com níveis de b-hCG baixos e persistentes configuram três situações distintas: a) havendo história anterior de DTG, a situação é classificada como DTG quiescente; b) sem antecedente de DTG, é configurada uma elevação inexplicada de hCG e c) os casos falso-positivos, também chamados de “hCG fantasma”.
hCG na monitorização do tratamento quimioterápico
Durante a monitorização do tratamento com Qt é essencial a manutenção das dosagens quantitativas e semanais de hCG. A resposta adequada à Qt é facilmente verificada pela análise da curva de regressão do hCG, a qual regride paralelamente à curva padrão. Entretanto, se estiver se desenvolvendo resistência ao agente quimioterápico utilizado, os valores do hCG voltam a ficar em plateau ou ascendentes, o que indica mudança de esquema de Qt.
Vale destacar que, no início do tratamento com qualquer fármaco quimioterápico, freqüentemente se observa um pequeno aumento nos valores séricos do hCG porque, devido à lise das células tumorais, ocorre mais liberação de gonadotrofina coriônica na circulação sanguínea, refletida pelo aumento inicial no hCG.
hCG no diagnóstico de NTG recidivante
A manutenção do controle do hCG precisa persistir após o final do tratamento com ou sem Qt, com a finalidade de precocemente ser diagnosticada uma recidiva de NTG
Após a remissão da NTG, momento em que se iniciam os ciclos de reforço ou consolidação do tratamento com Qt, as dosagens de hCG devem seguir sendo realizadas a cada 15 dias, até o final das séries de Qt e recuperação hematológica.
A recidiva da NTG varia de menos de 5% a 20%, de acordo com o estadiamento da FIGO, respectivamente nos estádios I e IV. Considerando que 80% das recidivas de NTG acontecem nos primeiros 3 meses após a remissão, nesse período a dosagem de hCG precisa ser feita a cada 15 dias. Após esses 3 meses, o controle laboratorial do hCG passa a ser mensal por mais 6 meses e depois a cada 60 dias, por mais 6 meses.
O grupo liderado por Bagshawe recomenda posteriormente um controle semestral de hCG, até completar 5 anos da remissão, momento em que as pacientes com NTG não-metastática recebem alta do acompanhamento. Também recomendam que as pacientes com NTG metastática ou com diagnóstico de coriocarcinoma permaneçam com dosagem anual da gonadotrofina coriônica por um tempo indefinido, pelo risco mínimo, porém existente, de reativação tardia. Informações recentes (Seckl M; XIX World Congresso on GTD, Amsterdam, 2017) sugerem que esse controle tardio pode ser encerrado 7 anos após a remissão.
Leitura suplementar
Harvey RA. Measurement of human Chorionic Gonadotrophin (hCG) in the management of trophoblastic disease. In: Hancock BW, Seckl MJ and Berkowitz RS eds. Gestational Trophoblastic Disease – 4th edition, 2015, chapter 5- www/isstd/org
Uberti EMH, Diestel MCF, Campestrini DT et al. Importância e dificuldades na quantificação do bHCG em pacientes com Doença Trofoblástica Gestacional. GO Atual 1999;8(9):8-18.
Vartiainen J, Alfthan H, Lehtovirta P et al. Elevated hCG and a high proportion of hCG b in serum preceding the diagnosis of trophoblastic disease by seven months. Br J Obstet Gynaecol RCOG 2002;109:589-90.
Levavi H, Neri A, Bar J et al. “Hook effect” in complete hydatidiform molar pregnancy: a falsely low level of b-hCG. Obstet Gynecol 1993; 82:720-1.
Schlaerth JB, Morrow CP, Kletzky AO, et al. Prognostic characteristics of serum human chorionic gonadotropin titer regression following Molar Pregnancy. Obstet Gynecol 1981;50:478-82.
Maestá I, Rudge MVC, Passos JRS et al. Características das curvas de regressão da gonadotrofina coriônica pós-Mola Hidatiforme completa. RBGO 2000; 22(6):373-80.
Feltmate CM, Batorfi J, Fulop V et al. Human chorionic gonadotropin follow-up in patients with molar pregnancy: a time for reevaluation. Obstet Gynecol 2003; 101:732-6.
Kohorn EI. Persistent low-level “real” human chorionic gonadotropin: a clinical challenge and a therapeutic dilemma. Gynecol Oncol 2002; 85:315-20.
ACOG Committee Opinion nº 278. Avoiding inappropriate clinical decisions based on false-positive human chorionic test results. Obstet Gynecol 2002;100:1057-9.
Bagshawe KD. Choriocarcinoma: a model for tumour markers. Acta Oncol 1992;31:99-106.
Surwit EA, Hammond CB. Recurrent Gestational Trophoblastic Disease. Gynecol Oncol 1981; 12:177-85.
Souza JMQ, Braga A, Santos RS, Ramos MM, Cortez-Charry R, Maesta I. Comparison of two human chorionic gonadotropin immunoassay commercially available for monitoring patients with gestational trophoblastic disease. Int J Gynecol Cancer. 2017 Sep;27(7):1494-1500.
Comissão Nacional Especializada em Doença Trofoblástica Gestacional
FEBRASGO
Gestão 2016-2018
Elza Uberti, José Mauro Madi, Antonio Braga, Bruno Grillo, Maurício Viggiano,
Izildinha Maestá, Jurandyr Moreira de Andrade, Sue Sun, Rita de Cássia Ferreira
Para otimizar sua experiência durante a navegação, fazemos uso de cookies. Ao continuar no site consideramos que você está de acordo com a nossa Política de Privacidade.
Aceitar e continuar no site